醫(yī)藥網(wǎng)2月27日訊 醫(yī)保報銷水平和范圍不斷提升和擴大,,醫(yī)保基金壓力仍存,。2月19日,,國新辦舉行癌癥防治工作和藥品稅收優(yōu)惠政策吹風會上,國家醫(yī)療保障局醫(yī)藥服務管理司司長熊先軍透露:& 開展2019年醫(yī)保藥品目錄的調整工作,。將以切實保障參保人員基本醫(yī)療權益為目標,,以提升醫(yī)保基金使用效率為核心,,做好臨床需求和醫(yī)?;鸪惺苣芰χg的平衡,將更多符合條件的救急救命的好藥按照規(guī)定的程序納入醫(yī)保藥品目錄,,不斷提升基本醫(yī)療保障水平,。&
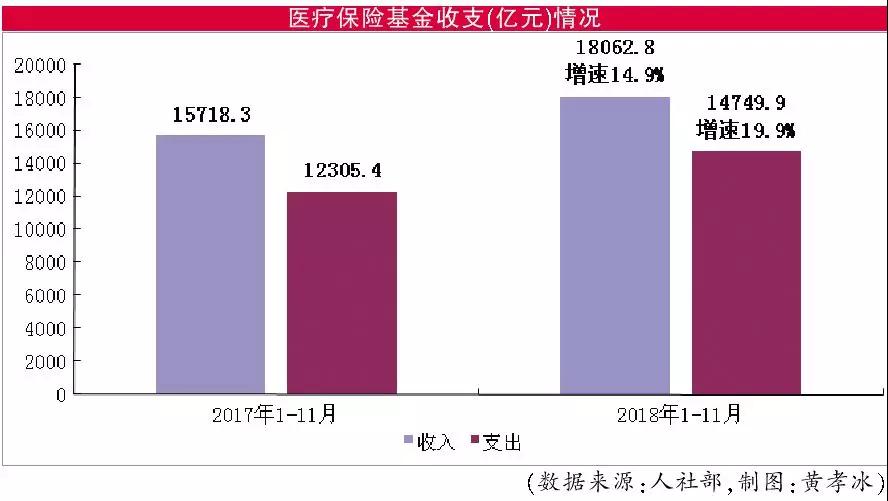 醫(yī)保基金承壓
把高價抗癌藥納入醫(yī)保,,觸及民生熱點,,正是各地& 兩會& 上代表委員們密切關注的熱點話題。我國將加快醫(yī)保藥品目錄調整頻率,,把更多救命救急的抗癌藥納入醫(yī)保,,被業(yè)內點評為是我國醫(yī)保目錄動態(tài)調整機制建設進入加速期的信號。江蘇省政協(xié)委員,、省醫(yī)療保障局副局長相伯偉表示,,江蘇省已將兩批合計31種抗癌藥納入醫(yī)保基金支付范圍,,近5.5萬名患者率先受益,。
去年以來,我國采取一系列措施提高抗癌藥的可及性,。2018年10月,,我國將包括奧希替尼在內的17種抗癌藥納入《國家基本醫(yī)療保險、工傷保險和生育保險藥品目錄(2017年版)》乙類范圍,,醫(yī)保支付標準較零售價平均降幅達56.7%,。
據(jù)新華社最新消息,截至去年底,,全國醫(yī)療機構和藥店按談判價格采購17種國家談判抗癌藥總量約為184萬粒(片/支),,采購總金額5.62億元,與談判前價格相比節(jié)省采購費用9.18億元,,醫(yī)保報銷后費用負擔降低超過75%,。
劍指& 看病貴& ,,醫(yī)保支付方式改革已然進入深化期。然而,,醫(yī)保基金面臨很大壓力,。報道顯示,我國醫(yī)?;鹬С鲈鏊僖呀咏?0%,,高于基金收入增速,。& 醫(yī)保基金的支出具有剛性,,醫(yī)保基金支出增速高于收入增速,,醫(yī)?;饓毫M一步增加,。& 中國社科院人口與勞動經(jīng)濟研究所社會保障研究室專家在接受媒體采訪時表示,。
& 為確保患者能夠用得起高價藥,,可通過多方共付和多措并舉加以解決。& 清華大學醫(yī)療管理研究中心研究員黃燕在接受《醫(yī)藥經(jīng)濟報》記者采訪時指出,,& 多方共付,就是由財政,、醫(yī)保,、慈善捐款和個人共同支付高價藥。其中,,患者自費的比例應該是最低的,經(jīng)濟困難群體則可享受價格補貼,,或者全免費。多措并舉,,目的是讓高價藥合理降價,,并規(guī)范和合理使用高價藥,比如對高價藥實行政府談判,、集中帶量采購等,,同時嚴格規(guī)范高價藥的使用和監(jiān)管等,。&
記者留意到,,國家醫(yī)保局有關負責人曾明確表示,,為讓患者享受到更多好藥,又不讓醫(yī)?;鸪霈F(xiàn)嚴重赤字,將通過價格談判來降低藥價,,將藥價中不合理的部分擠掉,。2月19日,,上海發(fā)布《關于本市做好國家組織藥品集中采購和使用試點有關工作的通知》提出,對一些高價抗癌藥適當提高個人自負比例,。
抗癌藥研發(fā)提速
抗腫瘤藥等新藥研發(fā)也是& 兩會& 關注點。全國政協(xié)委員,、中科院化學研究所研究員王春儒提出,目前,,美國癌癥患者的五年生存率達70%,,而我國不足30%,,原因在于我國缺乏治癌新藥。因此,,我國加強癌癥等重大疾病防治攻關迫在眉睫,。
山東省人大代表、魯南制藥集團董事長張貴民對媒體表示,,從目前申請通過的新藥批文來看,山東醫(yī)藥企業(yè)比較少,。期待加大新藥研發(fā)扶持力度,,給企業(yè)更大的支持,政府可用風投基金介入新藥研發(fā),。
業(yè)內有分析指出,隨著國家政策鼓勵創(chuàng)新藥,、資本爭相進入和大批海歸& 回巢& ,,中國抗癌藥研發(fā)正進入百舸爭流的競技狀態(tài),,不斷縮小與歐美國家的差距,。未來中國將有大批抗腫瘤藥物上市,除了高端仿制藥,,還有創(chuàng)新藥,,中國癌癥患者生存率也將有所提升。
記者注意到,,藥品審評審批制度改革以來,新藥上市速度已大幅加快,。國家藥品監(jiān)督管理局藥品注冊司相關負責人在2月19日國務院政策例行吹風會上透露,,從審批數(shù)量來看,2018年批準抗癌新藥18個,,比2017年增長157%。從審批的品種結構來看,,2018年批準的抗癌新藥占全年批準新藥總數(shù)的37.5%,,也顯著高于往年。從審批速度來看,,2018年以前,,我國抗癌新藥審批平均用時24個月,現(xiàn)在平均12個月左右,,我國與發(fā)達國家的審批速度日趨一致,。九價HPV疫苗,,從新藥申請到獲批,只用了8天,,創(chuàng)新藥進口注冊獲批最快記錄,;中國批準首款PD-1抗癌藥從提交上市申請到獲批,也僅用了9個月時間,。
2018年我國批準了多個自主創(chuàng)新的抗癌新藥,,如非小細胞肺癌用藥鹽酸安羅替尼膠囊、復發(fā)或轉移性乳腺癌治療藥物馬來酸吡咯替尼片,、轉移性結直腸癌藥物呋喹替尼膠囊,以及2個國產(chǎn)PD-1單抗,。
市場層面,,從第二批36個談判品種放量情況來看,進入醫(yī)保目錄后,,絕大多數(shù)品種的市場有比較明顯的增長。用于難治的外周T細胞淋巴瘤的抗癌藥西達本胺,,談判成功后,,2018年第一季度銷量與去年同期相比增長285倍,。
在政策和市場導向下,越來越多的藥企布局抗癌藥市場,。截至2018年12月10日,,國家藥監(jiān)局藥品審評中心總計接收并處理申請人溝通交流申請1500余個,其中,,抗腫瘤藥物的申請600余個。
醫(yī)保基金承壓
把高價抗癌藥納入醫(yī)保,,觸及民生熱點,,正是各地& 兩會& 上代表委員們密切關注的熱點話題。我國將加快醫(yī)保藥品目錄調整頻率,,把更多救命救急的抗癌藥納入醫(yī)保,,被業(yè)內點評為是我國醫(yī)保目錄動態(tài)調整機制建設進入加速期的信號。江蘇省政協(xié)委員,、省醫(yī)療保障局副局長相伯偉表示,,江蘇省已將兩批合計31種抗癌藥納入醫(yī)保基金支付范圍,,近5.5萬名患者率先受益,。
去年以來,我國采取一系列措施提高抗癌藥的可及性,。2018年10月,,我國將包括奧希替尼在內的17種抗癌藥納入《國家基本醫(yī)療保險、工傷保險和生育保險藥品目錄(2017年版)》乙類范圍,,醫(yī)保支付標準較零售價平均降幅達56.7%,。
據(jù)新華社最新消息,截至去年底,,全國醫(yī)療機構和藥店按談判價格采購17種國家談判抗癌藥總量約為184萬粒(片/支),,采購總金額5.62億元,與談判前價格相比節(jié)省采購費用9.18億元,,醫(yī)保報銷后費用負擔降低超過75%,。
劍指& 看病貴& ,,醫(yī)保支付方式改革已然進入深化期。然而,,醫(yī)保基金面臨很大壓力,。報道顯示,我國醫(yī)?;鹬С鲈鏊僖呀咏?0%,,高于基金收入增速,。& 醫(yī)保基金的支出具有剛性,,醫(yī)保基金支出增速高于收入增速,,醫(yī)?;饓毫M一步增加,。& 中國社科院人口與勞動經(jīng)濟研究所社會保障研究室專家在接受媒體采訪時表示,。
& 為確保患者能夠用得起高價藥,,可通過多方共付和多措并舉加以解決。& 清華大學醫(yī)療管理研究中心研究員黃燕在接受《醫(yī)藥經(jīng)濟報》記者采訪時指出,,& 多方共付,就是由財政,、醫(yī)保,、慈善捐款和個人共同支付高價藥。其中,,患者自費的比例應該是最低的,經(jīng)濟困難群體則可享受價格補貼,,或者全免費。多措并舉,,目的是讓高價藥合理降價,,并規(guī)范和合理使用高價藥,比如對高價藥實行政府談判,、集中帶量采購等,,同時嚴格規(guī)范高價藥的使用和監(jiān)管等,。&
記者留意到,,國家醫(yī)保局有關負責人曾明確表示,,為讓患者享受到更多好藥,又不讓醫(yī)?;鸪霈F(xiàn)嚴重赤字,將通過價格談判來降低藥價,,將藥價中不合理的部分擠掉,。2月19日,,上海發(fā)布《關于本市做好國家組織藥品集中采購和使用試點有關工作的通知》提出,對一些高價抗癌藥適當提高個人自負比例,。
抗癌藥研發(fā)提速
抗腫瘤藥等新藥研發(fā)也是& 兩會& 關注點。全國政協(xié)委員,、中科院化學研究所研究員王春儒提出,目前,,美國癌癥患者的五年生存率達70%,,而我國不足30%,,原因在于我國缺乏治癌新藥。因此,,我國加強癌癥等重大疾病防治攻關迫在眉睫,。
山東省人大代表、魯南制藥集團董事長張貴民對媒體表示,,從目前申請通過的新藥批文來看,山東醫(yī)藥企業(yè)比較少,。期待加大新藥研發(fā)扶持力度,,給企業(yè)更大的支持,政府可用風投基金介入新藥研發(fā),。
業(yè)內有分析指出,隨著國家政策鼓勵創(chuàng)新藥,、資本爭相進入和大批海歸& 回巢& ,,中國抗癌藥研發(fā)正進入百舸爭流的競技狀態(tài),,不斷縮小與歐美國家的差距,。未來中國將有大批抗腫瘤藥物上市,除了高端仿制藥,,還有創(chuàng)新藥,,中國癌癥患者生存率也將有所提升。
記者注意到,,藥品審評審批制度改革以來,新藥上市速度已大幅加快,。國家藥品監(jiān)督管理局藥品注冊司相關負責人在2月19日國務院政策例行吹風會上透露,,從審批數(shù)量來看,2018年批準抗癌新藥18個,,比2017年增長157%。從審批的品種結構來看,,2018年批準的抗癌新藥占全年批準新藥總數(shù)的37.5%,,也顯著高于往年。從審批速度來看,,2018年以前,,我國抗癌新藥審批平均用時24個月,現(xiàn)在平均12個月左右,,我國與發(fā)達國家的審批速度日趨一致,。九價HPV疫苗,,從新藥申請到獲批,只用了8天,,創(chuàng)新藥進口注冊獲批最快記錄,;中國批準首款PD-1抗癌藥從提交上市申請到獲批,也僅用了9個月時間,。
2018年我國批準了多個自主創(chuàng)新的抗癌新藥,,如非小細胞肺癌用藥鹽酸安羅替尼膠囊、復發(fā)或轉移性乳腺癌治療藥物馬來酸吡咯替尼片,、轉移性結直腸癌藥物呋喹替尼膠囊,以及2個國產(chǎn)PD-1單抗,。
市場層面,,從第二批36個談判品種放量情況來看,進入醫(yī)保目錄后,,絕大多數(shù)品種的市場有比較明顯的增長。用于難治的外周T細胞淋巴瘤的抗癌藥西達本胺,,談判成功后,,2018年第一季度銷量與去年同期相比增長285倍,。
在政策和市場導向下,越來越多的藥企布局抗癌藥市場,。截至2018年12月10日,,國家藥監(jiān)局藥品審評中心總計接收并處理申請人溝通交流申請1500余個,其中,,抗腫瘤藥物的申請600余個。
 醫(yī)保基金承壓
把高價抗癌藥納入醫(yī)保,,觸及民生熱點,,正是各地& 兩會& 上代表委員們密切關注的熱點話題。我國將加快醫(yī)保藥品目錄調整頻率,,把更多救命救急的抗癌藥納入醫(yī)保,,被業(yè)內點評為是我國醫(yī)保目錄動態(tài)調整機制建設進入加速期的信號。江蘇省政協(xié)委員,、省醫(yī)療保障局副局長相伯偉表示,,江蘇省已將兩批合計31種抗癌藥納入醫(yī)保基金支付范圍,,近5.5萬名患者率先受益,。
去年以來,我國采取一系列措施提高抗癌藥的可及性,。2018年10月,,我國將包括奧希替尼在內的17種抗癌藥納入《國家基本醫(yī)療保險、工傷保險和生育保險藥品目錄(2017年版)》乙類范圍,,醫(yī)保支付標準較零售價平均降幅達56.7%,。
據(jù)新華社最新消息,截至去年底,,全國醫(yī)療機構和藥店按談判價格采購17種國家談判抗癌藥總量約為184萬粒(片/支),,采購總金額5.62億元,與談判前價格相比節(jié)省采購費用9.18億元,,醫(yī)保報銷后費用負擔降低超過75%,。
劍指& 看病貴& ,,醫(yī)保支付方式改革已然進入深化期。然而,,醫(yī)保基金面臨很大壓力,。報道顯示,我國醫(yī)?;鹬С鲈鏊僖呀咏?0%,,高于基金收入增速,。& 醫(yī)保基金的支出具有剛性,,醫(yī)保基金支出增速高于收入增速,,醫(yī)?;饓毫M一步增加,。& 中國社科院人口與勞動經(jīng)濟研究所社會保障研究室專家在接受媒體采訪時表示,。
& 為確保患者能夠用得起高價藥,,可通過多方共付和多措并舉加以解決。& 清華大學醫(yī)療管理研究中心研究員黃燕在接受《醫(yī)藥經(jīng)濟報》記者采訪時指出,,& 多方共付,就是由財政,、醫(yī)保,、慈善捐款和個人共同支付高價藥。其中,,患者自費的比例應該是最低的,經(jīng)濟困難群體則可享受價格補貼,,或者全免費。多措并舉,,目的是讓高價藥合理降價,,并規(guī)范和合理使用高價藥,比如對高價藥實行政府談判,、集中帶量采購等,,同時嚴格規(guī)范高價藥的使用和監(jiān)管等,。&
記者留意到,,國家醫(yī)保局有關負責人曾明確表示,,為讓患者享受到更多好藥,又不讓醫(yī)?;鸪霈F(xiàn)嚴重赤字,將通過價格談判來降低藥價,,將藥價中不合理的部分擠掉,。2月19日,,上海發(fā)布《關于本市做好國家組織藥品集中采購和使用試點有關工作的通知》提出,對一些高價抗癌藥適當提高個人自負比例,。
抗癌藥研發(fā)提速
抗腫瘤藥等新藥研發(fā)也是& 兩會& 關注點。全國政協(xié)委員,、中科院化學研究所研究員王春儒提出,目前,,美國癌癥患者的五年生存率達70%,,而我國不足30%,,原因在于我國缺乏治癌新藥。因此,,我國加強癌癥等重大疾病防治攻關迫在眉睫,。
山東省人大代表、魯南制藥集團董事長張貴民對媒體表示,,從目前申請通過的新藥批文來看,山東醫(yī)藥企業(yè)比較少,。期待加大新藥研發(fā)扶持力度,,給企業(yè)更大的支持,政府可用風投基金介入新藥研發(fā),。
業(yè)內有分析指出,隨著國家政策鼓勵創(chuàng)新藥,、資本爭相進入和大批海歸& 回巢& ,,中國抗癌藥研發(fā)正進入百舸爭流的競技狀態(tài),,不斷縮小與歐美國家的差距,。未來中國將有大批抗腫瘤藥物上市,除了高端仿制藥,,還有創(chuàng)新藥,,中國癌癥患者生存率也將有所提升。
記者注意到,,藥品審評審批制度改革以來,新藥上市速度已大幅加快,。國家藥品監(jiān)督管理局藥品注冊司相關負責人在2月19日國務院政策例行吹風會上透露,,從審批數(shù)量來看,2018年批準抗癌新藥18個,,比2017年增長157%。從審批的品種結構來看,,2018年批準的抗癌新藥占全年批準新藥總數(shù)的37.5%,,也顯著高于往年。從審批速度來看,,2018年以前,,我國抗癌新藥審批平均用時24個月,現(xiàn)在平均12個月左右,,我國與發(fā)達國家的審批速度日趨一致,。九價HPV疫苗,,從新藥申請到獲批,只用了8天,,創(chuàng)新藥進口注冊獲批最快記錄,;中國批準首款PD-1抗癌藥從提交上市申請到獲批,也僅用了9個月時間,。
2018年我國批準了多個自主創(chuàng)新的抗癌新藥,,如非小細胞肺癌用藥鹽酸安羅替尼膠囊、復發(fā)或轉移性乳腺癌治療藥物馬來酸吡咯替尼片,、轉移性結直腸癌藥物呋喹替尼膠囊,以及2個國產(chǎn)PD-1單抗,。
市場層面,,從第二批36個談判品種放量情況來看,進入醫(yī)保目錄后,,絕大多數(shù)品種的市場有比較明顯的增長。用于難治的外周T細胞淋巴瘤的抗癌藥西達本胺,,談判成功后,,2018年第一季度銷量與去年同期相比增長285倍,。
在政策和市場導向下,越來越多的藥企布局抗癌藥市場,。截至2018年12月10日,,國家藥監(jiān)局藥品審評中心總計接收并處理申請人溝通交流申請1500余個,其中,,抗腫瘤藥物的申請600余個。
醫(yī)保基金承壓
把高價抗癌藥納入醫(yī)保,,觸及民生熱點,,正是各地& 兩會& 上代表委員們密切關注的熱點話題。我國將加快醫(yī)保藥品目錄調整頻率,,把更多救命救急的抗癌藥納入醫(yī)保,,被業(yè)內點評為是我國醫(yī)保目錄動態(tài)調整機制建設進入加速期的信號。江蘇省政協(xié)委員,、省醫(yī)療保障局副局長相伯偉表示,,江蘇省已將兩批合計31種抗癌藥納入醫(yī)保基金支付范圍,,近5.5萬名患者率先受益,。
去年以來,我國采取一系列措施提高抗癌藥的可及性,。2018年10月,,我國將包括奧希替尼在內的17種抗癌藥納入《國家基本醫(yī)療保險、工傷保險和生育保險藥品目錄(2017年版)》乙類范圍,,醫(yī)保支付標準較零售價平均降幅達56.7%,。
據(jù)新華社最新消息,截至去年底,,全國醫(yī)療機構和藥店按談判價格采購17種國家談判抗癌藥總量約為184萬粒(片/支),,采購總金額5.62億元,與談判前價格相比節(jié)省采購費用9.18億元,,醫(yī)保報銷后費用負擔降低超過75%,。
劍指& 看病貴& ,,醫(yī)保支付方式改革已然進入深化期。然而,,醫(yī)保基金面臨很大壓力,。報道顯示,我國醫(yī)?;鹬С鲈鏊僖呀咏?0%,,高于基金收入增速,。& 醫(yī)保基金的支出具有剛性,,醫(yī)保基金支出增速高于收入增速,,醫(yī)?;饓毫M一步增加,。& 中國社科院人口與勞動經(jīng)濟研究所社會保障研究室專家在接受媒體采訪時表示,。
& 為確保患者能夠用得起高價藥,,可通過多方共付和多措并舉加以解決。& 清華大學醫(yī)療管理研究中心研究員黃燕在接受《醫(yī)藥經(jīng)濟報》記者采訪時指出,,& 多方共付,就是由財政,、醫(yī)保,、慈善捐款和個人共同支付高價藥。其中,,患者自費的比例應該是最低的,經(jīng)濟困難群體則可享受價格補貼,,或者全免費。多措并舉,,目的是讓高價藥合理降價,,并規(guī)范和合理使用高價藥,比如對高價藥實行政府談判,、集中帶量采購等,,同時嚴格規(guī)范高價藥的使用和監(jiān)管等,。&
記者留意到,,國家醫(yī)保局有關負責人曾明確表示,,為讓患者享受到更多好藥,又不讓醫(yī)?;鸪霈F(xiàn)嚴重赤字,將通過價格談判來降低藥價,,將藥價中不合理的部分擠掉,。2月19日,,上海發(fā)布《關于本市做好國家組織藥品集中采購和使用試點有關工作的通知》提出,對一些高價抗癌藥適當提高個人自負比例,。
抗癌藥研發(fā)提速
抗腫瘤藥等新藥研發(fā)也是& 兩會& 關注點。全國政協(xié)委員,、中科院化學研究所研究員王春儒提出,目前,,美國癌癥患者的五年生存率達70%,,而我國不足30%,,原因在于我國缺乏治癌新藥。因此,,我國加強癌癥等重大疾病防治攻關迫在眉睫,。
山東省人大代表、魯南制藥集團董事長張貴民對媒體表示,,從目前申請通過的新藥批文來看,山東醫(yī)藥企業(yè)比較少,。期待加大新藥研發(fā)扶持力度,,給企業(yè)更大的支持,政府可用風投基金介入新藥研發(fā),。
業(yè)內有分析指出,隨著國家政策鼓勵創(chuàng)新藥,、資本爭相進入和大批海歸& 回巢& ,,中國抗癌藥研發(fā)正進入百舸爭流的競技狀態(tài),,不斷縮小與歐美國家的差距,。未來中國將有大批抗腫瘤藥物上市,除了高端仿制藥,,還有創(chuàng)新藥,,中國癌癥患者生存率也將有所提升。
記者注意到,,藥品審評審批制度改革以來,新藥上市速度已大幅加快,。國家藥品監(jiān)督管理局藥品注冊司相關負責人在2月19日國務院政策例行吹風會上透露,,從審批數(shù)量來看,2018年批準抗癌新藥18個,,比2017年增長157%。從審批的品種結構來看,,2018年批準的抗癌新藥占全年批準新藥總數(shù)的37.5%,,也顯著高于往年。從審批速度來看,,2018年以前,,我國抗癌新藥審批平均用時24個月,現(xiàn)在平均12個月左右,,我國與發(fā)達國家的審批速度日趨一致,。九價HPV疫苗,,從新藥申請到獲批,只用了8天,,創(chuàng)新藥進口注冊獲批最快記錄,;中國批準首款PD-1抗癌藥從提交上市申請到獲批,也僅用了9個月時間,。
2018年我國批準了多個自主創(chuàng)新的抗癌新藥,,如非小細胞肺癌用藥鹽酸安羅替尼膠囊、復發(fā)或轉移性乳腺癌治療藥物馬來酸吡咯替尼片,、轉移性結直腸癌藥物呋喹替尼膠囊,以及2個國產(chǎn)PD-1單抗,。
市場層面,,從第二批36個談判品種放量情況來看,進入醫(yī)保目錄后,,絕大多數(shù)品種的市場有比較明顯的增長。用于難治的外周T細胞淋巴瘤的抗癌藥西達本胺,,談判成功后,,2018年第一季度銷量與去年同期相比增長285倍,。
在政策和市場導向下,越來越多的藥企布局抗癌藥市場,。截至2018年12月10日,,國家藥監(jiān)局藥品審評中心總計接收并處理申請人溝通交流申請1500余個,其中,,抗腫瘤藥物的申請600余個。







