日前,,恒瑞醫(yī)藥按仿制藥4類申報(bào)的注射用替莫唑胺獲批生產(chǎn),視同通過(guò)一致性評(píng)價(jià),。注射劑一致性評(píng)價(jià)雖然還沒(méi)有正式文件明確具體執(zhí)行時(shí)間節(jié)點(diǎn),,但已有不少企業(yè)提前布局。據(jù)米內(nèi)網(wǎng)數(shù)據(jù),,截至目前,,已有34家企業(yè)(以集團(tuán)計(jì),下同)布局注射劑一致性評(píng)價(jià),,共申報(bào)157個(gè)品規(guī)(涉及67個(gè)品種),,齊魯、恒瑞,、正大制藥,、科倫等企業(yè)走在前沿,靠的是什么妙招,?
表1:注射劑一致性評(píng)價(jià)申報(bào)品種數(shù)TOP10企業(yè)
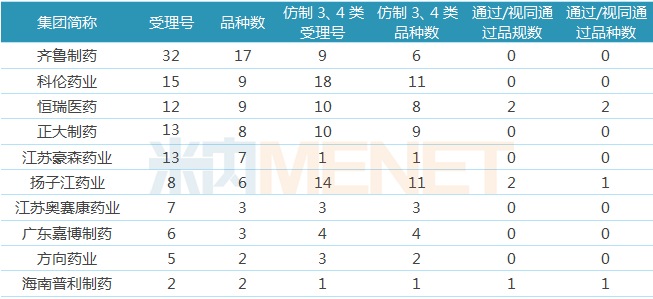
(來(lái)源:米內(nèi)網(wǎng)MED中國(guó)藥品審評(píng)數(shù)據(jù)庫(kù)2.0,,下同)
2017年12月22日,CDE發(fā)布《已上市化學(xué)仿制藥(注射劑)一致性評(píng)價(jià)技術(shù)要求(征求意見(jiàn)稿)》,,雖然只是“技術(shù)要求”文件,,未明確具體執(zhí)行時(shí)間節(jié)點(diǎn)、范圍等,,但這預(yù)示著,,注射劑一致性評(píng)價(jià)已被納入日程,即將開(kāi)展,!
據(jù)米內(nèi)網(wǎng)數(shù)據(jù),,2017年中國(guó)公立醫(yī)療機(jī)構(gòu)終端注射劑市場(chǎng)接近6000億元,在注射劑一致性評(píng)價(jià)真正來(lái)臨之前,,已有不少企業(yè)搶先布局,。截至1月16日,,已有34家企業(yè)布局注射劑一致性評(píng)價(jià),共申報(bào)157個(gè)品規(guī)(涉及67個(gè)品種),。齊魯制藥,、恒瑞醫(yī)藥、正大制藥,、豪森藥業(yè),、科倫藥業(yè)的注射劑一致性評(píng)價(jià)補(bǔ)充申請(qǐng)受理號(hào)均超過(guò)10個(gè),其中齊魯制藥以32個(gè)受理號(hào),、17個(gè)品種數(shù)遙遙領(lǐng)先,。
4大藥企,“國(guó)外轉(zhuǎn)報(bào)國(guó)內(nèi)”彎道超車
根據(jù)國(guó)家藥監(jiān)局發(fā)布的2016年第106號(hào)文件:“國(guó)內(nèi)藥品生產(chǎn)企業(yè)已在歐盟,、美國(guó)和日本獲準(zhǔn)上市的仿制藥,,可以國(guó)外注冊(cè)申報(bào)的相關(guān)資料為基礎(chǔ),按照化學(xué)藥品新注冊(cè)分類申報(bào)藥品上市,,批準(zhǔn)上市后視同通過(guò)一致性評(píng)價(jià),;在中國(guó)境內(nèi)用同一生產(chǎn)線生產(chǎn)上市并在歐盟、美國(guó)和日本獲準(zhǔn)上市的藥品,,視同通過(guò)一致性評(píng)價(jià)”,。這讓國(guó)內(nèi)企業(yè)在美國(guó)申報(bào)ANDA后轉(zhuǎn)報(bào)國(guó)內(nèi)一致性評(píng)價(jià)成為了一條現(xiàn)實(shí)可行的路徑,也確實(shí)有越來(lái)越多的企業(yè)沿著這樣一條路徑付出實(shí)際行動(dòng),。
“已有化藥注射劑出口到國(guó)際主流市場(chǎng)的企業(yè),,將先一步完成一致性評(píng)價(jià)并取得市場(chǎng)優(yōu)勢(shì)?!鄙虾J惺称?strong>藥品檢驗(yàn)所謝沐風(fēng)副主任藥師認(rèn)為,,出口企業(yè)在生產(chǎn)技術(shù)和產(chǎn)品質(zhì)量方面已取得歐美日等地區(qū)和國(guó)家認(rèn)證,這為其產(chǎn)品進(jìn)行一致性評(píng)價(jià)打下了良好基礎(chǔ),。
表2:齊魯制藥注射劑一致性評(píng)價(jià)申請(qǐng)情況
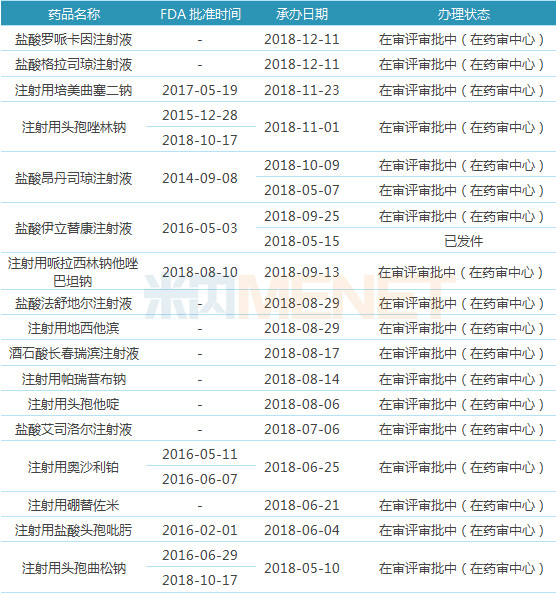
齊魯制藥注射劑一致性評(píng)價(jià)受理號(hào)32個(gè),,涉及品種17個(gè),其中有8個(gè)品種已在美國(guó)獲得ANDA文號(hào),,這8個(gè)品種以國(guó)外注冊(cè)申報(bào)的相關(guān)資料進(jìn)行申報(bào),,無(wú)需再進(jìn)行BE試驗(yàn);此外鹽酸帕洛諾司瓊注射液等品種也已獲得ANDA,,后續(xù)有望轉(zhuǎn)報(bào)國(guó)內(nèi),。按仿制藥3類、4類申報(bào)的注射劑的受理號(hào)有9個(gè),,涉及品種6個(gè),獲批生產(chǎn)后視同通過(guò)一致性評(píng)價(jià),。
表3:恒瑞醫(yī)藥注射劑一致性評(píng)價(jià)申請(qǐng)情況
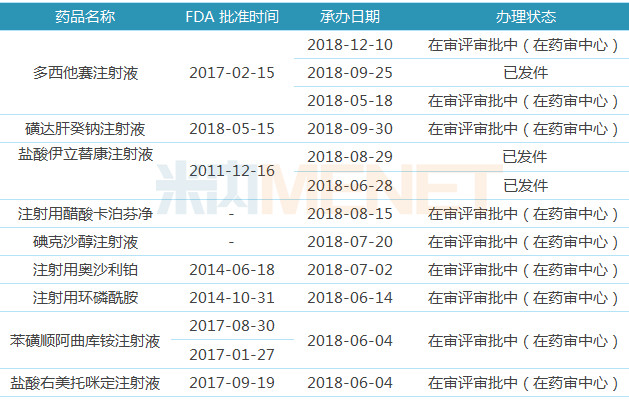
恒瑞醫(yī)藥注射劑一致性評(píng)價(jià)受理號(hào)12個(gè),,涉及品種9個(gè),,其中有7個(gè)品種已在美國(guó)獲得ANDA文號(hào),這7個(gè)品種以國(guó)外注冊(cè)申報(bào)的相關(guān)資料進(jìn)行申報(bào),,無(wú)需再進(jìn)行BE試驗(yàn),;此外鹽酸右美托咪定注射液、塞替派注射液等品種也已獲得ANDA,,后續(xù)有望轉(zhuǎn)報(bào)國(guó)內(nèi),。
按仿制藥3類、4類申報(bào)的注射劑的受理號(hào)有10個(gè),,涉及品種8個(gè),,其中按4類申報(bào)的注射用替莫唑胺已于日前獲批生產(chǎn),目前已被納入《中國(guó)上市藥品目錄集》,,視同通過(guò)一致性評(píng)價(jià),,據(jù)米內(nèi)網(wǎng)數(shù)據(jù),2017年中國(guó)公立醫(yī)療機(jī)構(gòu)終端替莫唑胺銷售額為18.55億元,,在恒瑞的產(chǎn)品獲批之前未有注射劑上市銷售,;注射用紫杉醇(白蛋白結(jié)合型)雖按仿制藥6類申報(bào),但獲批生產(chǎn)后被納入《中國(guó)上市藥品目錄集》,,視同通過(guò)一致性評(píng)價(jià),。
表4:豪森藥業(yè)注射劑一致性評(píng)價(jià)申請(qǐng)情況
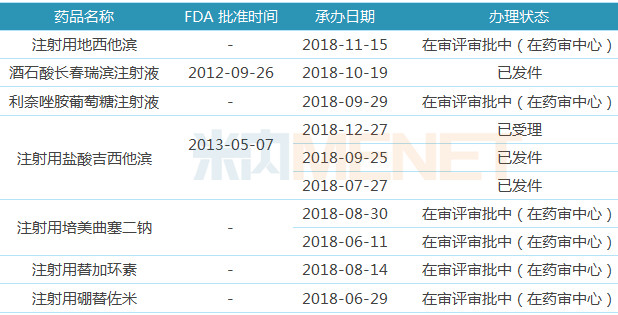
豪森藥業(yè)注射劑一致性評(píng)價(jià)受理號(hào)13個(gè),涉及品種7個(gè),,其中注射用鹽酸吉西他濱,、酒石酸長(zhǎng)春瑞濱注射液已在美國(guó)獲得ANDA文號(hào),以國(guó)外注冊(cè)申報(bào)的相關(guān)資料進(jìn)行申報(bào),,無(wú)需再進(jìn)行BE試驗(yàn),;按仿制藥3類、4類申報(bào)的注射劑的受理號(hào)有1個(gè),,涉及品種1個(gè),,獲批生產(chǎn)后視同通過(guò)一致性評(píng)價(jià)。
表5:普利制藥注射劑一致性評(píng)價(jià)申請(qǐng)情況

普利制藥注射劑一致性評(píng)價(jià)受理號(hào)2個(gè),,涉及品種2個(gè),,均已在美國(guó)獲得ANDA文號(hào),以國(guó)外注冊(cè)申報(bào)的相關(guān)資料進(jìn)行申報(bào),,無(wú)需再進(jìn)行BE試驗(yàn),;注射用阿奇霉素已順利通過(guò)一致性評(píng)價(jià),成為首個(gè)通過(guò)一致性評(píng)價(jià)補(bǔ)充申請(qǐng)獲得批準(zhǔn)的注射劑,。此外左乙拉西坦注射液,、注射用伏立康唑等品種已在美國(guó)獲得ANDA文號(hào),后續(xù)有望轉(zhuǎn)報(bào)國(guó)內(nèi),,其中注射用伏立康唑已按仿制藥4類申報(bào)上市,,獲批生產(chǎn)后視同通過(guò)一致性評(píng)價(jià),。
科倫藥業(yè),大輸液龍頭盡顯優(yōu)勢(shì)
據(jù)科倫藥業(yè)年報(bào)數(shù)據(jù),,2017年公司實(shí)現(xiàn)營(yíng)業(yè)收入114.35億元,,同比上年增長(zhǎng)33.49%,其中輸液產(chǎn)品實(shí)現(xiàn)銷售收入75.79億元,,同比上年增長(zhǎng)26.12%,,輸液板塊占公司總營(yíng)業(yè)收入比重為66.28%。
據(jù)CDE已發(fā)布的注射劑一致性評(píng)價(jià)技術(shù)要求文件,,氯化鈉注射液,、葡萄糖注射液等普通大輸液原則上不納入一致性評(píng)價(jià)范圍,但可能會(huì)在滅菌工藝等方面做一些其他要求,,這意味著科倫藥業(yè)的幾款重磅產(chǎn)品不需要進(jìn)行一致性評(píng)價(jià),。據(jù)米內(nèi)網(wǎng)數(shù)據(jù),科倫藥業(yè)的氯化鈉注射液,、葡萄糖注射液,、葡萄糖氯化鈉注射液在2017年中國(guó)公立醫(yī)療機(jī)構(gòu)終端的銷售額分別為35.64億元、19.79億元,、7.34億元,。
表6:科倫藥業(yè)注射劑一致性評(píng)價(jià)申請(qǐng)情況
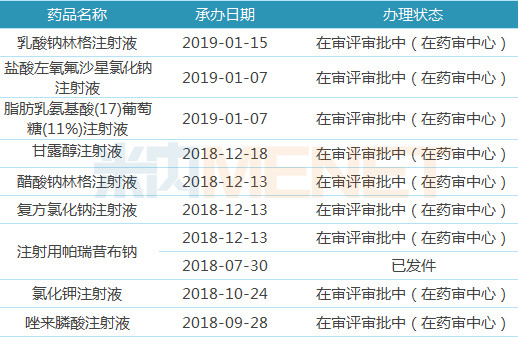
除普通大輸液外,治療性輸液是需要納入一致性評(píng)價(jià)的,,目前科倫藥業(yè)已提交并受到CDE承辦的注射劑一致性評(píng)價(jià)申請(qǐng)受理號(hào)有15個(gè),,涉及品種數(shù)9個(gè)。
表7:科倫藥業(yè)按新3類,、4類申報(bào)的注射劑
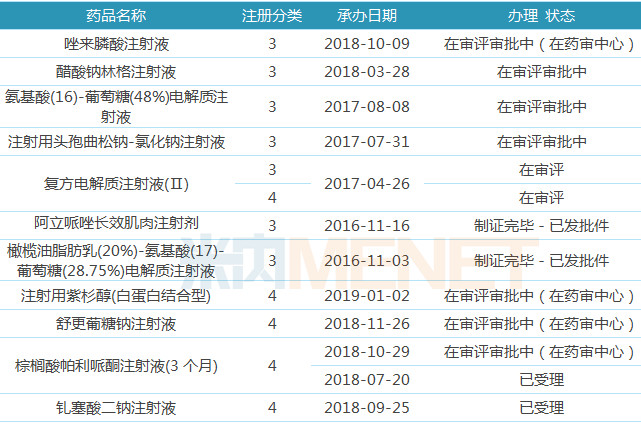
按仿制藥3類,、4類申報(bào)的注射劑的受理號(hào)有18個(gè),涉及品種11個(gè),,阿立哌唑長(zhǎng)效肌肉注射劑已獲批臨床,,國(guó)內(nèi)暫無(wú)該產(chǎn)品上市銷售;舒更葡糖鈉注射液,、棕櫚酸帕利哌酮注射液,、釓塞酸二鈉注射液、復(fù)方電解質(zhì)注射液(Ⅱ)等品種目前只有原研廠家的產(chǎn)品在國(guó)內(nèi)銷售,。
來(lái)源:米內(nèi)網(wǎng)數(shù)據(jù)庫(kù)
注:數(shù)據(jù)統(tǒng)計(jì)截至1月16日







