潤(rùn)寶醫(yī)療網(wǎng)6月22日訊 1、一級(jí)召回 6月18日,,國(guó)家藥監(jiān)局發(fā)布了一則關(guān)于對(duì)主動(dòng)脈內(nèi)球囊反搏泵主動(dòng)召回的通告,。  通告內(nèi)容中指出:泰利福醫(yī)療器械商貿(mào)(上海)有限公司報(bào)告,由于涉及產(chǎn)品可能存在IABP中一個(gè)組件易受振動(dòng)故障的影響,,最終引起突然停止運(yùn)行或無(wú)法啟動(dòng)IABP的問(wèn)題,,生產(chǎn)商箭牌國(guó)際公司Arrow International, Inc.對(duì)主動(dòng)脈內(nèi)球囊反搏泵(商品名:AutoCAT 2,、AutoCAT 2 WAVE)(注冊(cè)證編號(hào):國(guó)械注進(jìn)20153211603,、國(guó)械注進(jìn)20153081603、國(guó)食藥監(jiān)械(進(jìn))字2011第3211652號(hào))主動(dòng)召回,。 此次召回的產(chǎn)品共計(jì)694臺(tái),,召回級(jí)別為一級(jí),涉及產(chǎn)品的名稱,、注冊(cè)證或備案憑證編碼,、型號(hào),、規(guī)格及批次等詳細(xì)信息見《醫(yī)療器械召回事件報(bào)告表》。 2017年5月起執(zhí)行《醫(yī)療器械召回管理辦法》中明確,,使用該醫(yī)療器械可能或者已經(jīng)引起嚴(yán)重健康危害的,,實(shí)施一級(jí)召回;可能或者已經(jīng)引起暫時(shí)的,、可逆的健康危害的,,實(shí)施二級(jí)召回;引起危害的可能性較小但仍需要召回的,,實(shí)施三級(jí)召回,。 同時(shí),醫(yī)療器械生產(chǎn)企業(yè)作出醫(yī)療器械召回決定的,,一級(jí)召回應(yīng)當(dāng)在1日內(nèi),;二級(jí)召回應(yīng)當(dāng)在3日內(nèi);三級(jí)召回應(yīng)當(dāng)在7日內(nèi)通知到有關(guān)醫(yī)療器械經(jīng)營(yíng)企業(yè),、使用單位或者告知使用者,。
通告內(nèi)容中指出:泰利福醫(yī)療器械商貿(mào)(上海)有限公司報(bào)告,由于涉及產(chǎn)品可能存在IABP中一個(gè)組件易受振動(dòng)故障的影響,,最終引起突然停止運(yùn)行或無(wú)法啟動(dòng)IABP的問(wèn)題,,生產(chǎn)商箭牌國(guó)際公司Arrow International, Inc.對(duì)主動(dòng)脈內(nèi)球囊反搏泵(商品名:AutoCAT 2,、AutoCAT 2 WAVE)(注冊(cè)證編號(hào):國(guó)械注進(jìn)20153211603,、國(guó)械注進(jìn)20153081603、國(guó)食藥監(jiān)械(進(jìn))字2011第3211652號(hào))主動(dòng)召回,。 此次召回的產(chǎn)品共計(jì)694臺(tái),,召回級(jí)別為一級(jí),涉及產(chǎn)品的名稱,、注冊(cè)證或備案憑證編碼,、型號(hào),、規(guī)格及批次等詳細(xì)信息見《醫(yī)療器械召回事件報(bào)告表》。 2017年5月起執(zhí)行《醫(yī)療器械召回管理辦法》中明確,,使用該醫(yī)療器械可能或者已經(jīng)引起嚴(yán)重健康危害的,,實(shí)施一級(jí)召回;可能或者已經(jīng)引起暫時(shí)的,、可逆的健康危害的,,實(shí)施二級(jí)召回;引起危害的可能性較小但仍需要召回的,,實(shí)施三級(jí)召回,。 同時(shí),醫(yī)療器械生產(chǎn)企業(yè)作出醫(yī)療器械召回決定的,,一級(jí)召回應(yīng)當(dāng)在1日內(nèi),;二級(jí)召回應(yīng)當(dāng)在3日內(nèi);三級(jí)召回應(yīng)當(dāng)在7日內(nèi)通知到有關(guān)醫(yī)療器械經(jīng)營(yíng)企業(yè),、使用單位或者告知使用者,。 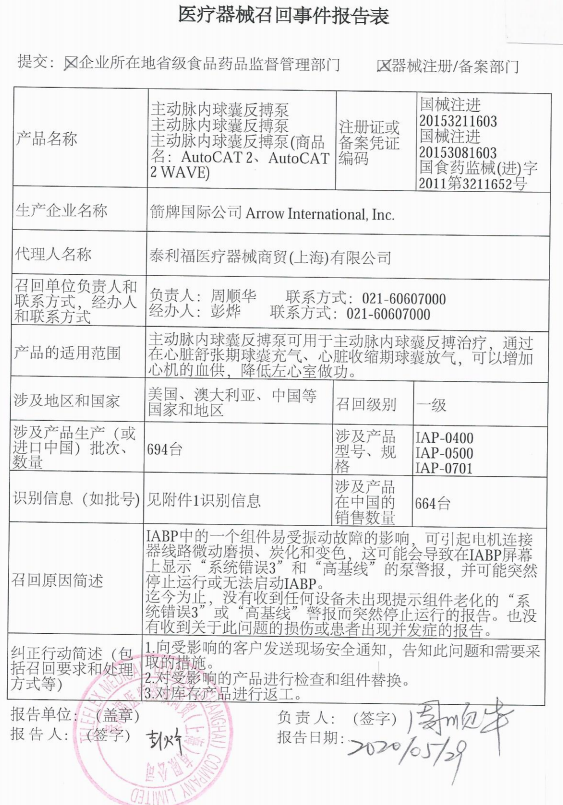 2、11批次醫(yī)療器械將召回 日前,,河南省藥品監(jiān)督管理局網(wǎng)站發(fā)布醫(yī)療器械質(zhì)量公告(2020年第2期)。據(jù)公告,,一次性使用電子控制鎮(zhèn)痛泵等11批次產(chǎn)品不符合標(biāo)準(zhǔn)規(guī)定,。
2、11批次醫(yī)療器械將召回 日前,,河南省藥品監(jiān)督管理局網(wǎng)站發(fā)布醫(yī)療器械質(zhì)量公告(2020年第2期)。據(jù)公告,,一次性使用電子控制鎮(zhèn)痛泵等11批次產(chǎn)品不符合標(biāo)準(zhǔn)規(guī)定,。  為加強(qiáng)醫(yī)療器械質(zhì)量監(jiān)督管理,保障醫(yī)療器械產(chǎn)品使用安全有效,,河南省藥品監(jiān)督管理局對(duì)全省生產(chǎn),、經(jīng)營(yíng)、使用環(huán)節(jié)的醫(yī)療器械產(chǎn)品組織了監(jiān)督抽檢,。 河南省藥品監(jiān)督管理局表示,,對(duì)不符合標(biāo)準(zhǔn)規(guī)定產(chǎn)品,已按程序移交企業(yè)所在地監(jiān)督管理部門,,相關(guān)生產(chǎn),、經(jīng)營(yíng)企業(yè)按有關(guān)法律法規(guī)要求召回并進(jìn)行風(fēng)險(xiǎn)控制,企業(yè)所在地監(jiān)督管理部門要依法調(diào)查處置,,有關(guān)處置情況及時(shí)向社會(huì)公布,。
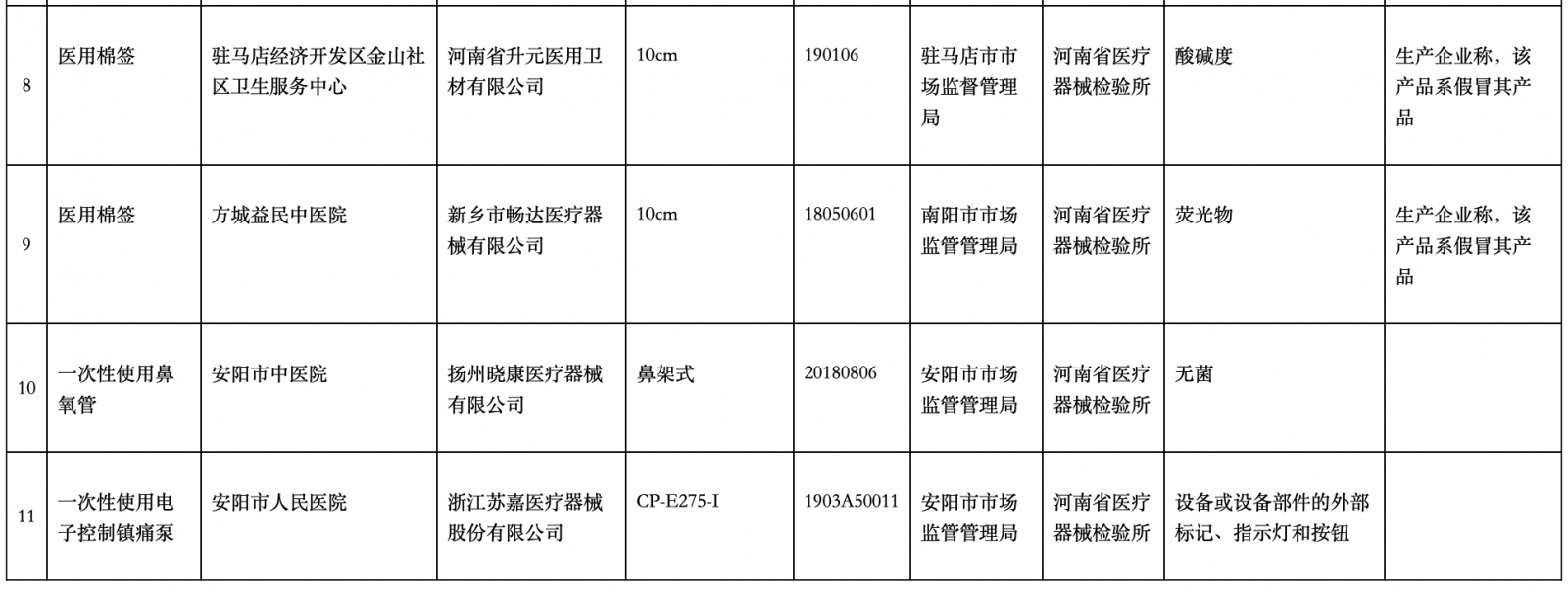
為加強(qiáng)醫(yī)療器械質(zhì)量監(jiān)督管理,保障醫(yī)療器械產(chǎn)品使用安全有效,,河南省藥品監(jiān)督管理局對(duì)全省生產(chǎn),、經(jīng)營(yíng)、使用環(huán)節(jié)的醫(yī)療器械產(chǎn)品組織了監(jiān)督抽檢,。 河南省藥品監(jiān)督管理局表示,,對(duì)不符合標(biāo)準(zhǔn)規(guī)定產(chǎn)品,已按程序移交企業(yè)所在地監(jiān)督管理部門,,相關(guān)生產(chǎn),、經(jīng)營(yíng)企業(yè)按有關(guān)法律法規(guī)要求召回并進(jìn)行風(fēng)險(xiǎn)控制,企業(yè)所在地監(jiān)督管理部門要依法調(diào)查處置,,有關(guān)處置情況及時(shí)向社會(huì)公布,。 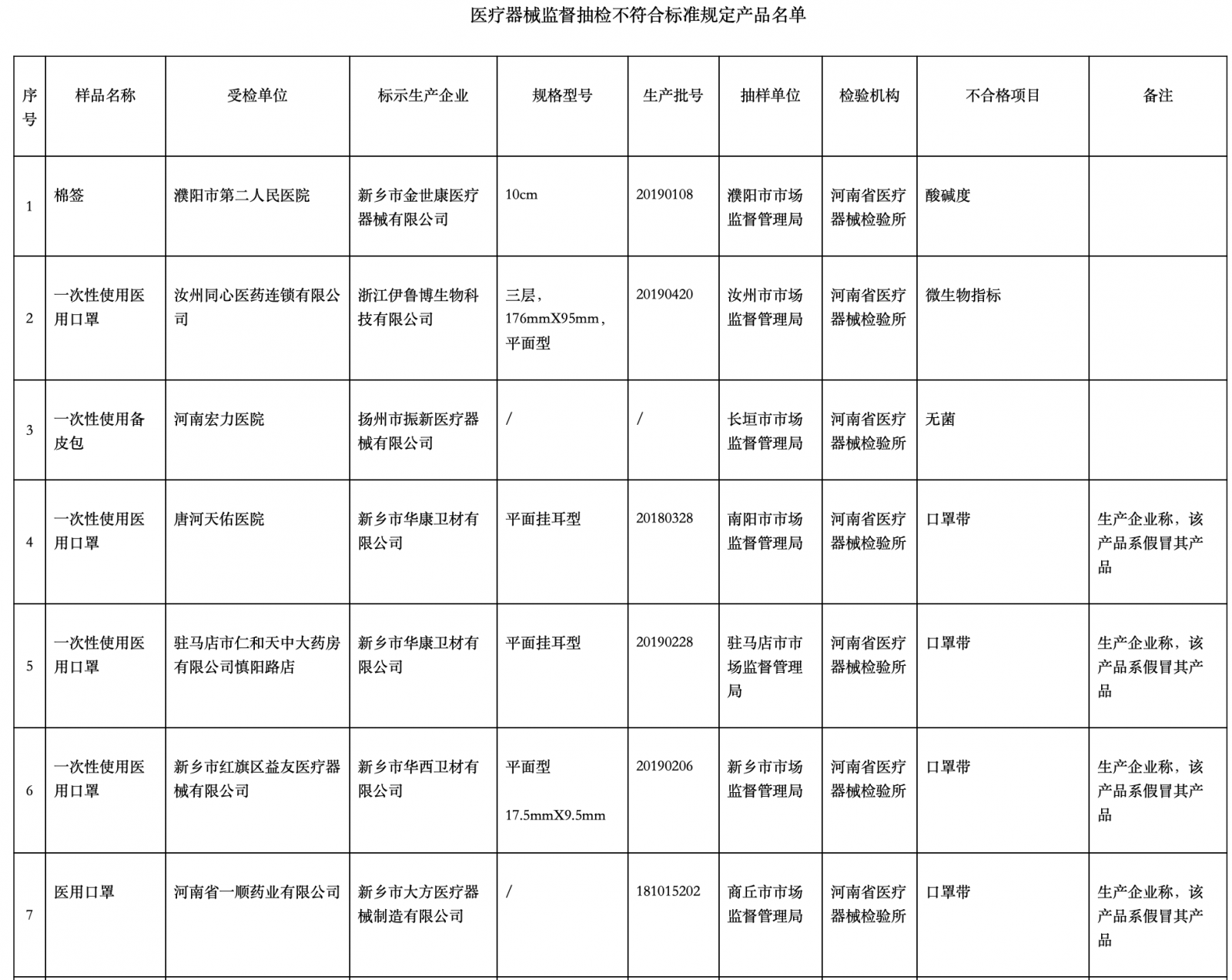
 通告內(nèi)容中指出:泰利福醫(yī)療器械商貿(mào)(上海)有限公司報(bào)告,由于涉及產(chǎn)品可能存在IABP中一個(gè)組件易受振動(dòng)故障的影響,,最終引起突然停止運(yùn)行或無(wú)法啟動(dòng)IABP的問(wèn)題,,生產(chǎn)商箭牌國(guó)際公司Arrow International, Inc.對(duì)主動(dòng)脈內(nèi)球囊反搏泵(商品名:AutoCAT 2,、AutoCAT 2 WAVE)(注冊(cè)證編號(hào):國(guó)械注進(jìn)20153211603,、國(guó)械注進(jìn)20153081603、國(guó)食藥監(jiān)械(進(jìn))字2011第3211652號(hào))主動(dòng)召回,。 此次召回的產(chǎn)品共計(jì)694臺(tái),,召回級(jí)別為一級(jí),涉及產(chǎn)品的名稱,、注冊(cè)證或備案憑證編碼,、型號(hào),、規(guī)格及批次等詳細(xì)信息見《醫(yī)療器械召回事件報(bào)告表》。 2017年5月起執(zhí)行《醫(yī)療器械召回管理辦法》中明確,,使用該醫(yī)療器械可能或者已經(jīng)引起嚴(yán)重健康危害的,,實(shí)施一級(jí)召回;可能或者已經(jīng)引起暫時(shí)的,、可逆的健康危害的,,實(shí)施二級(jí)召回;引起危害的可能性較小但仍需要召回的,,實(shí)施三級(jí)召回,。 同時(shí),醫(yī)療器械生產(chǎn)企業(yè)作出醫(yī)療器械召回決定的,,一級(jí)召回應(yīng)當(dāng)在1日內(nèi),;二級(jí)召回應(yīng)當(dāng)在3日內(nèi);三級(jí)召回應(yīng)當(dāng)在7日內(nèi)通知到有關(guān)醫(yī)療器械經(jīng)營(yíng)企業(yè),、使用單位或者告知使用者,。
通告內(nèi)容中指出:泰利福醫(yī)療器械商貿(mào)(上海)有限公司報(bào)告,由于涉及產(chǎn)品可能存在IABP中一個(gè)組件易受振動(dòng)故障的影響,,最終引起突然停止運(yùn)行或無(wú)法啟動(dòng)IABP的問(wèn)題,,生產(chǎn)商箭牌國(guó)際公司Arrow International, Inc.對(duì)主動(dòng)脈內(nèi)球囊反搏泵(商品名:AutoCAT 2,、AutoCAT 2 WAVE)(注冊(cè)證編號(hào):國(guó)械注進(jìn)20153211603,、國(guó)械注進(jìn)20153081603、國(guó)食藥監(jiān)械(進(jìn))字2011第3211652號(hào))主動(dòng)召回,。 此次召回的產(chǎn)品共計(jì)694臺(tái),,召回級(jí)別為一級(jí),涉及產(chǎn)品的名稱,、注冊(cè)證或備案憑證編碼,、型號(hào),、規(guī)格及批次等詳細(xì)信息見《醫(yī)療器械召回事件報(bào)告表》。 2017年5月起執(zhí)行《醫(yī)療器械召回管理辦法》中明確,,使用該醫(yī)療器械可能或者已經(jīng)引起嚴(yán)重健康危害的,,實(shí)施一級(jí)召回;可能或者已經(jīng)引起暫時(shí)的,、可逆的健康危害的,,實(shí)施二級(jí)召回;引起危害的可能性較小但仍需要召回的,,實(shí)施三級(jí)召回,。 同時(shí),醫(yī)療器械生產(chǎn)企業(yè)作出醫(yī)療器械召回決定的,,一級(jí)召回應(yīng)當(dāng)在1日內(nèi),;二級(jí)召回應(yīng)當(dāng)在3日內(nèi);三級(jí)召回應(yīng)當(dāng)在7日內(nèi)通知到有關(guān)醫(yī)療器械經(jīng)營(yíng)企業(yè),、使用單位或者告知使用者,。  2、11批次醫(yī)療器械將召回 日前,,河南省藥品監(jiān)督管理局網(wǎng)站發(fā)布醫(yī)療器械質(zhì)量公告(2020年第2期)。據(jù)公告,,一次性使用電子控制鎮(zhèn)痛泵等11批次產(chǎn)品不符合標(biāo)準(zhǔn)規(guī)定,。
2、11批次醫(yī)療器械將召回 日前,,河南省藥品監(jiān)督管理局網(wǎng)站發(fā)布醫(yī)療器械質(zhì)量公告(2020年第2期)。據(jù)公告,,一次性使用電子控制鎮(zhèn)痛泵等11批次產(chǎn)品不符合標(biāo)準(zhǔn)規(guī)定,。  為加強(qiáng)醫(yī)療器械質(zhì)量監(jiān)督管理,保障醫(yī)療器械產(chǎn)品使用安全有效,,河南省藥品監(jiān)督管理局對(duì)全省生產(chǎn),、經(jīng)營(yíng)、使用環(huán)節(jié)的醫(yī)療器械產(chǎn)品組織了監(jiān)督抽檢,。 河南省藥品監(jiān)督管理局表示,,對(duì)不符合標(biāo)準(zhǔn)規(guī)定產(chǎn)品,已按程序移交企業(yè)所在地監(jiān)督管理部門,,相關(guān)生產(chǎn),、經(jīng)營(yíng)企業(yè)按有關(guān)法律法規(guī)要求召回并進(jìn)行風(fēng)險(xiǎn)控制,企業(yè)所在地監(jiān)督管理部門要依法調(diào)查處置,,有關(guān)處置情況及時(shí)向社會(huì)公布,。
為加強(qiáng)醫(yī)療器械質(zhì)量監(jiān)督管理,保障醫(yī)療器械產(chǎn)品使用安全有效,,河南省藥品監(jiān)督管理局對(duì)全省生產(chǎn),、經(jīng)營(yíng)、使用環(huán)節(jié)的醫(yī)療器械產(chǎn)品組織了監(jiān)督抽檢,。 河南省藥品監(jiān)督管理局表示,,對(duì)不符合標(biāo)準(zhǔn)規(guī)定產(chǎn)品,已按程序移交企業(yè)所在地監(jiān)督管理部門,,相關(guān)生產(chǎn),、經(jīng)營(yíng)企業(yè)按有關(guān)法律法規(guī)要求召回并進(jìn)行風(fēng)險(xiǎn)控制,企業(yè)所在地監(jiān)督管理部門要依法調(diào)查處置,,有關(guān)處置情況及時(shí)向社會(huì)公布,。 




