醫(yī)藥網(wǎng)1月22日訊 日前,,CDE發(fā)布新一批擬優(yōu)先審評(píng)產(chǎn)品信息,有6個(gè)受理號(hào)(涉及3個(gè)品種,,3家企業(yè))擬納入優(yōu)先審評(píng),,有望加速上市,。據(jù)悉,3個(gè)品種均以& 具有明顯治療優(yōu)勢(shì)& 為由擬納入優(yōu)先審評(píng),。
表1:擬納入優(yōu)先審評(píng)品種
 (來源:CDE官網(wǎng))
深圳微芯生物科技的西達(dá)本胺片,,以新藥2.4的注冊(cè)類型申報(bào)上市,受理號(hào)為CXHS1800033,,推測(cè)適應(yīng)癥為乳腺癌,。2014年12月,深圳微芯生物科技的西達(dá)本胺片以新藥1.1申報(bào)上市并獲得國家藥監(jiān)局批準(zhǔn),,獲批的適應(yīng)癥是T細(xì)胞淋巴瘤,。
圖1:2015-2017年中國公立醫(yī)療機(jī)構(gòu)終端西達(dá)本胺片銷售情況(單位:萬元)
(來源:CDE官網(wǎng))
深圳微芯生物科技的西達(dá)本胺片,,以新藥2.4的注冊(cè)類型申報(bào)上市,受理號(hào)為CXHS1800033,,推測(cè)適應(yīng)癥為乳腺癌,。2014年12月,深圳微芯生物科技的西達(dá)本胺片以新藥1.1申報(bào)上市并獲得國家藥監(jiān)局批準(zhǔn),,獲批的適應(yīng)癥是T細(xì)胞淋巴瘤,。
圖1:2015-2017年中國公立醫(yī)療機(jī)構(gòu)終端西達(dá)本胺片銷售情況(單位:萬元)
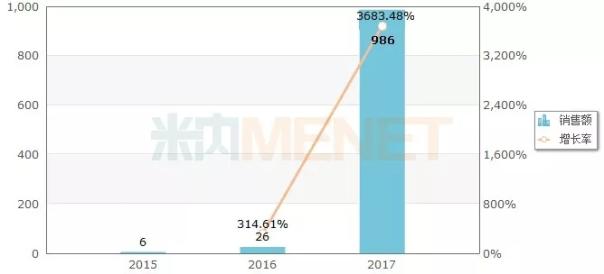 (來源:米內(nèi)網(wǎng)中國公立醫(yī)療機(jī)構(gòu)終端競(jìng)爭(zhēng)格局)
據(jù)米內(nèi)網(wǎng)數(shù)據(jù),目前國內(nèi)市場(chǎng)上市銷售西達(dá)本胺片的企業(yè)僅深圳微芯生物科技一家,,該公司產(chǎn)品自上市銷售以來,,銷售額呈現(xiàn)逐年遞增的態(tài)勢(shì),2018年有望突破1億元大關(guān),。
再鼎醫(yī)藥的對(duì)甲苯磺酸尼拉帕利及對(duì)甲苯磺酸尼拉帕利膠囊,,以新藥1類申報(bào)上市并獲得CDE受理承辦,受理號(hào)為CXHS1800042,、CXHS1800043,,該產(chǎn)品于2017年3月在國內(nèi)提交臨床申請(qǐng),同年7月獲批臨床,。
對(duì)甲苯磺酸尼拉帕利是一種高效,、選擇性的每日一次口服小分子聚(ADP-核糖)PARP 1/2抑制劑,基于在美國和歐洲的獲批,,再鼎醫(yī)藥在香港提交Niraparib的市場(chǎng)注冊(cè)申請(qǐng),,2018年10月22日,再鼎醫(yī)藥宣布,,公司研發(fā)的1類新藥對(duì)甲苯磺酸尼拉帕利膠囊(英文名Niraparib,,代號(hào)ZL-2306)在香港獲批上市,用于對(duì)含鉑化療完全緩解(CR)或部分緩解(PR)的鉑敏感復(fù)發(fā)性高級(jí)別漿液性的上皮卵巢癌患者的治療,。
Niraparib已于2017年3月在美國獲批,,成為FDA批準(zhǔn)上市的第三個(gè)PARP抑制劑,此前阿斯利康的Olaparib和Clovis的Rucaparib已經(jīng)上市,,用于BRCA變異復(fù)發(fā)卵巢癌的治療,。Niraparib是第一個(gè)用于維持治療的PARP抑制劑,即用于維持處于緩解階段的患者,,且Niraparib沒有BRCA變異限制,,所以適用人群大于前兩個(gè)PARP抑制劑;同年11月,,Niraparib在歐洲獲批,,用于維持治療對(duì)含鉑化療完全或部分緩解的復(fù)發(fā)性上皮卵巢癌,、輸卵管癌或原發(fā)性腹膜癌患者。
阿斯利康的布地奈德格隆溴銨福莫特羅吸入氣霧劑,,以進(jìn)口2.3的注冊(cè)類型提交上市申請(qǐng),,已獲得CDE受理承辦,受理號(hào)為JXHS1800033,、JXHS1800034,、JXHS1800035。布地奈德格隆溴銨福莫特羅吸入氣霧劑由一個(gè)吸入性糖皮質(zhì)激素,、一個(gè)長(zhǎng)效M受體拮抗劑以及一個(gè)長(zhǎng)效β2受體激動(dòng)劑組成,,支氣管擴(kuò)張作用會(huì)更強(qiáng)。目前該三方制劑尚未在全球上市,,中國有望首次批準(zhǔn),。
(來源:米內(nèi)網(wǎng)中國公立醫(yī)療機(jī)構(gòu)終端競(jìng)爭(zhēng)格局)
據(jù)米內(nèi)網(wǎng)數(shù)據(jù),目前國內(nèi)市場(chǎng)上市銷售西達(dá)本胺片的企業(yè)僅深圳微芯生物科技一家,,該公司產(chǎn)品自上市銷售以來,,銷售額呈現(xiàn)逐年遞增的態(tài)勢(shì),2018年有望突破1億元大關(guān),。
再鼎醫(yī)藥的對(duì)甲苯磺酸尼拉帕利及對(duì)甲苯磺酸尼拉帕利膠囊,,以新藥1類申報(bào)上市并獲得CDE受理承辦,受理號(hào)為CXHS1800042,、CXHS1800043,,該產(chǎn)品于2017年3月在國內(nèi)提交臨床申請(qǐng),同年7月獲批臨床,。
對(duì)甲苯磺酸尼拉帕利是一種高效,、選擇性的每日一次口服小分子聚(ADP-核糖)PARP 1/2抑制劑,基于在美國和歐洲的獲批,,再鼎醫(yī)藥在香港提交Niraparib的市場(chǎng)注冊(cè)申請(qǐng),,2018年10月22日,再鼎醫(yī)藥宣布,,公司研發(fā)的1類新藥對(duì)甲苯磺酸尼拉帕利膠囊(英文名Niraparib,,代號(hào)ZL-2306)在香港獲批上市,用于對(duì)含鉑化療完全緩解(CR)或部分緩解(PR)的鉑敏感復(fù)發(fā)性高級(jí)別漿液性的上皮卵巢癌患者的治療,。
Niraparib已于2017年3月在美國獲批,,成為FDA批準(zhǔn)上市的第三個(gè)PARP抑制劑,此前阿斯利康的Olaparib和Clovis的Rucaparib已經(jīng)上市,,用于BRCA變異復(fù)發(fā)卵巢癌的治療,。Niraparib是第一個(gè)用于維持治療的PARP抑制劑,即用于維持處于緩解階段的患者,,且Niraparib沒有BRCA變異限制,,所以適用人群大于前兩個(gè)PARP抑制劑;同年11月,,Niraparib在歐洲獲批,,用于維持治療對(duì)含鉑化療完全或部分緩解的復(fù)發(fā)性上皮卵巢癌,、輸卵管癌或原發(fā)性腹膜癌患者。
阿斯利康的布地奈德格隆溴銨福莫特羅吸入氣霧劑,,以進(jìn)口2.3的注冊(cè)類型提交上市申請(qǐng),,已獲得CDE受理承辦,受理號(hào)為JXHS1800033,、JXHS1800034,、JXHS1800035。布地奈德格隆溴銨福莫特羅吸入氣霧劑由一個(gè)吸入性糖皮質(zhì)激素,、一個(gè)長(zhǎng)效M受體拮抗劑以及一個(gè)長(zhǎng)效β2受體激動(dòng)劑組成,,支氣管擴(kuò)張作用會(huì)更強(qiáng)。目前該三方制劑尚未在全球上市,,中國有望首次批準(zhǔn),。
 (來源:CDE官網(wǎng))
深圳微芯生物科技的西達(dá)本胺片,,以新藥2.4的注冊(cè)類型申報(bào)上市,受理號(hào)為CXHS1800033,,推測(cè)適應(yīng)癥為乳腺癌,。2014年12月,深圳微芯生物科技的西達(dá)本胺片以新藥1.1申報(bào)上市并獲得國家藥監(jiān)局批準(zhǔn),,獲批的適應(yīng)癥是T細(xì)胞淋巴瘤,。
圖1:2015-2017年中國公立醫(yī)療機(jī)構(gòu)終端西達(dá)本胺片銷售情況(單位:萬元)
(來源:CDE官網(wǎng))
深圳微芯生物科技的西達(dá)本胺片,,以新藥2.4的注冊(cè)類型申報(bào)上市,受理號(hào)為CXHS1800033,,推測(cè)適應(yīng)癥為乳腺癌,。2014年12月,深圳微芯生物科技的西達(dá)本胺片以新藥1.1申報(bào)上市并獲得國家藥監(jiān)局批準(zhǔn),,獲批的適應(yīng)癥是T細(xì)胞淋巴瘤,。
圖1:2015-2017年中國公立醫(yī)療機(jī)構(gòu)終端西達(dá)本胺片銷售情況(單位:萬元)
 (來源:米內(nèi)網(wǎng)中國公立醫(yī)療機(jī)構(gòu)終端競(jìng)爭(zhēng)格局)
據(jù)米內(nèi)網(wǎng)數(shù)據(jù),目前國內(nèi)市場(chǎng)上市銷售西達(dá)本胺片的企業(yè)僅深圳微芯生物科技一家,,該公司產(chǎn)品自上市銷售以來,,銷售額呈現(xiàn)逐年遞增的態(tài)勢(shì),2018年有望突破1億元大關(guān),。
再鼎醫(yī)藥的對(duì)甲苯磺酸尼拉帕利及對(duì)甲苯磺酸尼拉帕利膠囊,,以新藥1類申報(bào)上市并獲得CDE受理承辦,受理號(hào)為CXHS1800042,、CXHS1800043,,該產(chǎn)品于2017年3月在國內(nèi)提交臨床申請(qǐng),同年7月獲批臨床,。
對(duì)甲苯磺酸尼拉帕利是一種高效,、選擇性的每日一次口服小分子聚(ADP-核糖)PARP 1/2抑制劑,基于在美國和歐洲的獲批,,再鼎醫(yī)藥在香港提交Niraparib的市場(chǎng)注冊(cè)申請(qǐng),,2018年10月22日,再鼎醫(yī)藥宣布,,公司研發(fā)的1類新藥對(duì)甲苯磺酸尼拉帕利膠囊(英文名Niraparib,,代號(hào)ZL-2306)在香港獲批上市,用于對(duì)含鉑化療完全緩解(CR)或部分緩解(PR)的鉑敏感復(fù)發(fā)性高級(jí)別漿液性的上皮卵巢癌患者的治療,。
Niraparib已于2017年3月在美國獲批,,成為FDA批準(zhǔn)上市的第三個(gè)PARP抑制劑,此前阿斯利康的Olaparib和Clovis的Rucaparib已經(jīng)上市,,用于BRCA變異復(fù)發(fā)卵巢癌的治療,。Niraparib是第一個(gè)用于維持治療的PARP抑制劑,即用于維持處于緩解階段的患者,,且Niraparib沒有BRCA變異限制,,所以適用人群大于前兩個(gè)PARP抑制劑;同年11月,,Niraparib在歐洲獲批,,用于維持治療對(duì)含鉑化療完全或部分緩解的復(fù)發(fā)性上皮卵巢癌,、輸卵管癌或原發(fā)性腹膜癌患者。
阿斯利康的布地奈德格隆溴銨福莫特羅吸入氣霧劑,,以進(jìn)口2.3的注冊(cè)類型提交上市申請(qǐng),,已獲得CDE受理承辦,受理號(hào)為JXHS1800033,、JXHS1800034,、JXHS1800035。布地奈德格隆溴銨福莫特羅吸入氣霧劑由一個(gè)吸入性糖皮質(zhì)激素,、一個(gè)長(zhǎng)效M受體拮抗劑以及一個(gè)長(zhǎng)效β2受體激動(dòng)劑組成,,支氣管擴(kuò)張作用會(huì)更強(qiáng)。目前該三方制劑尚未在全球上市,,中國有望首次批準(zhǔn),。
(來源:米內(nèi)網(wǎng)中國公立醫(yī)療機(jī)構(gòu)終端競(jìng)爭(zhēng)格局)
據(jù)米內(nèi)網(wǎng)數(shù)據(jù),目前國內(nèi)市場(chǎng)上市銷售西達(dá)本胺片的企業(yè)僅深圳微芯生物科技一家,,該公司產(chǎn)品自上市銷售以來,,銷售額呈現(xiàn)逐年遞增的態(tài)勢(shì),2018年有望突破1億元大關(guān),。
再鼎醫(yī)藥的對(duì)甲苯磺酸尼拉帕利及對(duì)甲苯磺酸尼拉帕利膠囊,,以新藥1類申報(bào)上市并獲得CDE受理承辦,受理號(hào)為CXHS1800042,、CXHS1800043,,該產(chǎn)品于2017年3月在國內(nèi)提交臨床申請(qǐng),同年7月獲批臨床,。
對(duì)甲苯磺酸尼拉帕利是一種高效,、選擇性的每日一次口服小分子聚(ADP-核糖)PARP 1/2抑制劑,基于在美國和歐洲的獲批,,再鼎醫(yī)藥在香港提交Niraparib的市場(chǎng)注冊(cè)申請(qǐng),,2018年10月22日,再鼎醫(yī)藥宣布,,公司研發(fā)的1類新藥對(duì)甲苯磺酸尼拉帕利膠囊(英文名Niraparib,,代號(hào)ZL-2306)在香港獲批上市,用于對(duì)含鉑化療完全緩解(CR)或部分緩解(PR)的鉑敏感復(fù)發(fā)性高級(jí)別漿液性的上皮卵巢癌患者的治療,。
Niraparib已于2017年3月在美國獲批,,成為FDA批準(zhǔn)上市的第三個(gè)PARP抑制劑,此前阿斯利康的Olaparib和Clovis的Rucaparib已經(jīng)上市,,用于BRCA變異復(fù)發(fā)卵巢癌的治療,。Niraparib是第一個(gè)用于維持治療的PARP抑制劑,即用于維持處于緩解階段的患者,,且Niraparib沒有BRCA變異限制,,所以適用人群大于前兩個(gè)PARP抑制劑;同年11月,,Niraparib在歐洲獲批,,用于維持治療對(duì)含鉑化療完全或部分緩解的復(fù)發(fā)性上皮卵巢癌,、輸卵管癌或原發(fā)性腹膜癌患者。
阿斯利康的布地奈德格隆溴銨福莫特羅吸入氣霧劑,,以進(jìn)口2.3的注冊(cè)類型提交上市申請(qǐng),,已獲得CDE受理承辦,受理號(hào)為JXHS1800033,、JXHS1800034,、JXHS1800035。布地奈德格隆溴銨福莫特羅吸入氣霧劑由一個(gè)吸入性糖皮質(zhì)激素,、一個(gè)長(zhǎng)效M受體拮抗劑以及一個(gè)長(zhǎng)效β2受體激動(dòng)劑組成,,支氣管擴(kuò)張作用會(huì)更強(qiáng)。目前該三方制劑尚未在全球上市,,中國有望首次批準(zhǔn),。







