醫(yī)藥網(wǎng)6月2日訊 5月31日,,普利制藥發(fā)布公告稱,公司于近日收到FDA簽發(fā)的注射用比伐蘆定仿制藥上市批準(zhǔn)通知,。該產(chǎn)品屬于公司共線生產(chǎn)的品種之一,,數(shù)據(jù)顯示,早前公司已拿下7個(gè)產(chǎn)品的ANDA文號,,對公司拓展美國市場帶來積極影響,。 表1:普利制藥獲批產(chǎn)品信息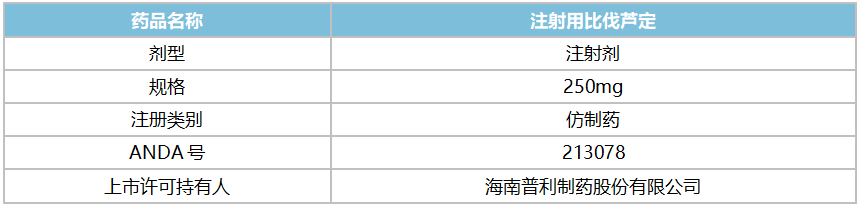 來源:公司公告 圖1:國內(nèi)市場上獲得注射用比伐蘆定生產(chǎn)批文的企業(yè)情況
來源:公司公告 圖1:國內(nèi)市場上獲得注射用比伐蘆定生產(chǎn)批文的企業(yè)情況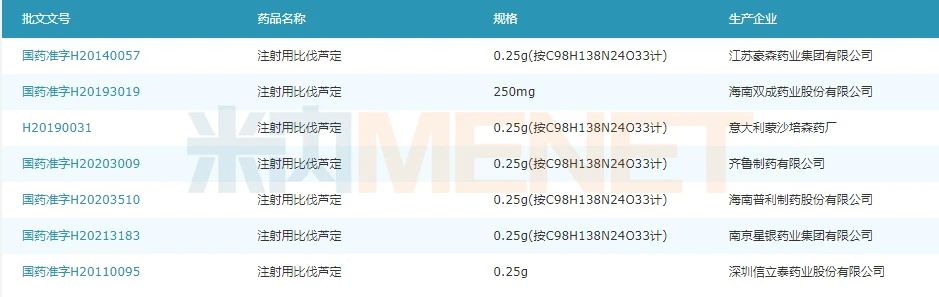 來源:米內(nèi)網(wǎng)一鍵檢索 注射用比伐蘆定是一種人工合成的抗凝血藥物,2020年在中國城市公立醫(yī)院,、縣級公立醫(yī)院,、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機(jī)構(gòu))終端銷售額超5億元,,海南普利制藥的4類仿制上市申請于2020年9月獲批并視同過評,,目前國內(nèi)市場上有7家藥企獲得該產(chǎn)品的生產(chǎn)批文(含1家原研進(jìn)口)。 普利制藥在公告中提到,,公司的注射用比伐蘆定屬于共線生產(chǎn)品種,,在2020年12月獲得FDA的暫時(shí)批準(zhǔn),目前美國原研產(chǎn)品還在專利保護(hù)期內(nèi),,專利期至2029年1月27日,。 普利制藥于2021年1月向FDA遞交了PIV專利(與所申請仿制藥相關(guān)的專利是無效的或仿制藥不侵權(quán))聲明,同時(shí)也向原研注射用比伐蘆定上市許可持有人和專利持有人發(fā)起專利挑戰(zhàn),,原研公司在收到通知后的45天內(nèi)未發(fā)起任何對普利制藥注射用比伐蘆定專利挑戰(zhàn)的訴訟,,即公司注射用比伐蘆定ANDA挑戰(zhàn)專利成功,隨后公司向FDA通報(bào)上述進(jìn)展并提交注射用比伐蘆定仿制藥最終上市批準(zhǔn)的申請,,近日公司收到FDA的上市批準(zhǔn)通知,,標(biāo)志著公司具備了在美國銷售注射用比伐蘆定的資格,。 表2:普利制藥早前已獲得的ANDA文號情況
來源:米內(nèi)網(wǎng)一鍵檢索 注射用比伐蘆定是一種人工合成的抗凝血藥物,2020年在中國城市公立醫(yī)院,、縣級公立醫(yī)院,、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機(jī)構(gòu))終端銷售額超5億元,,海南普利制藥的4類仿制上市申請于2020年9月獲批并視同過評,,目前國內(nèi)市場上有7家藥企獲得該產(chǎn)品的生產(chǎn)批文(含1家原研進(jìn)口)。 普利制藥在公告中提到,,公司的注射用比伐蘆定屬于共線生產(chǎn)品種,,在2020年12月獲得FDA的暫時(shí)批準(zhǔn),目前美國原研產(chǎn)品還在專利保護(hù)期內(nèi),,專利期至2029年1月27日,。 普利制藥于2021年1月向FDA遞交了PIV專利(與所申請仿制藥相關(guān)的專利是無效的或仿制藥不侵權(quán))聲明,同時(shí)也向原研注射用比伐蘆定上市許可持有人和專利持有人發(fā)起專利挑戰(zhàn),,原研公司在收到通知后的45天內(nèi)未發(fā)起任何對普利制藥注射用比伐蘆定專利挑戰(zhàn)的訴訟,,即公司注射用比伐蘆定ANDA挑戰(zhàn)專利成功,隨后公司向FDA通報(bào)上述進(jìn)展并提交注射用比伐蘆定仿制藥最終上市批準(zhǔn)的申請,,近日公司收到FDA的上市批準(zhǔn)通知,,標(biāo)志著公司具備了在美國銷售注射用比伐蘆定的資格,。 表2:普利制藥早前已獲得的ANDA文號情況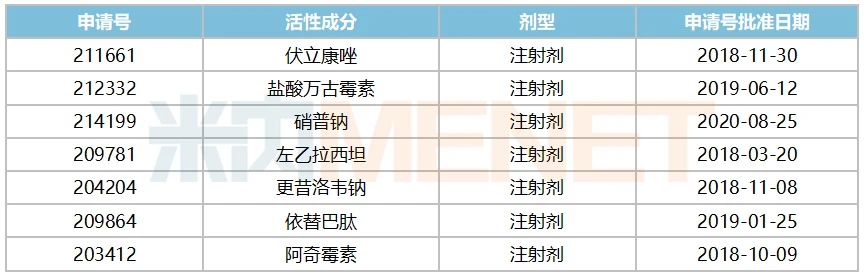 來源:米內(nèi)網(wǎng)全球上市藥物數(shù)據(jù)庫 據(jù)米內(nèi)網(wǎng)數(shù)據(jù)顯示,早前普利制藥已獲得了7個(gè)產(chǎn)品的ANDA文號,,本次注射用比伐蘆定獲批,,有助于提升公司在美國市場的銷售業(yè)績。 來源:公司公告,、米內(nèi)網(wǎng)數(shù)據(jù)庫
來源:米內(nèi)網(wǎng)全球上市藥物數(shù)據(jù)庫 據(jù)米內(nèi)網(wǎng)數(shù)據(jù)顯示,早前普利制藥已獲得了7個(gè)產(chǎn)品的ANDA文號,,本次注射用比伐蘆定獲批,,有助于提升公司在美國市場的銷售業(yè)績。 來源:公司公告,、米內(nèi)網(wǎng)數(shù)據(jù)庫
 來源:公司公告 圖1:國內(nèi)市場上獲得注射用比伐蘆定生產(chǎn)批文的企業(yè)情況
來源:公司公告 圖1:國內(nèi)市場上獲得注射用比伐蘆定生產(chǎn)批文的企業(yè)情況 來源:米內(nèi)網(wǎng)一鍵檢索 注射用比伐蘆定是一種人工合成的抗凝血藥物,2020年在中國城市公立醫(yī)院,、縣級公立醫(yī)院,、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機(jī)構(gòu))終端銷售額超5億元,,海南普利制藥的4類仿制上市申請于2020年9月獲批并視同過評,,目前國內(nèi)市場上有7家藥企獲得該產(chǎn)品的生產(chǎn)批文(含1家原研進(jìn)口)。 普利制藥在公告中提到,,公司的注射用比伐蘆定屬于共線生產(chǎn)品種,,在2020年12月獲得FDA的暫時(shí)批準(zhǔn),目前美國原研產(chǎn)品還在專利保護(hù)期內(nèi),,專利期至2029年1月27日,。 普利制藥于2021年1月向FDA遞交了PIV專利(與所申請仿制藥相關(guān)的專利是無效的或仿制藥不侵權(quán))聲明,同時(shí)也向原研注射用比伐蘆定上市許可持有人和專利持有人發(fā)起專利挑戰(zhàn),,原研公司在收到通知后的45天內(nèi)未發(fā)起任何對普利制藥注射用比伐蘆定專利挑戰(zhàn)的訴訟,,即公司注射用比伐蘆定ANDA挑戰(zhàn)專利成功,隨后公司向FDA通報(bào)上述進(jìn)展并提交注射用比伐蘆定仿制藥最終上市批準(zhǔn)的申請,,近日公司收到FDA的上市批準(zhǔn)通知,,標(biāo)志著公司具備了在美國銷售注射用比伐蘆定的資格,。 表2:普利制藥早前已獲得的ANDA文號情況
來源:米內(nèi)網(wǎng)一鍵檢索 注射用比伐蘆定是一種人工合成的抗凝血藥物,2020年在中國城市公立醫(yī)院,、縣級公立醫(yī)院,、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機(jī)構(gòu))終端銷售額超5億元,,海南普利制藥的4類仿制上市申請于2020年9月獲批并視同過評,,目前國內(nèi)市場上有7家藥企獲得該產(chǎn)品的生產(chǎn)批文(含1家原研進(jìn)口)。 普利制藥在公告中提到,,公司的注射用比伐蘆定屬于共線生產(chǎn)品種,,在2020年12月獲得FDA的暫時(shí)批準(zhǔn),目前美國原研產(chǎn)品還在專利保護(hù)期內(nèi),,專利期至2029年1月27日,。 普利制藥于2021年1月向FDA遞交了PIV專利(與所申請仿制藥相關(guān)的專利是無效的或仿制藥不侵權(quán))聲明,同時(shí)也向原研注射用比伐蘆定上市許可持有人和專利持有人發(fā)起專利挑戰(zhàn),,原研公司在收到通知后的45天內(nèi)未發(fā)起任何對普利制藥注射用比伐蘆定專利挑戰(zhàn)的訴訟,,即公司注射用比伐蘆定ANDA挑戰(zhàn)專利成功,隨后公司向FDA通報(bào)上述進(jìn)展并提交注射用比伐蘆定仿制藥最終上市批準(zhǔn)的申請,,近日公司收到FDA的上市批準(zhǔn)通知,,標(biāo)志著公司具備了在美國銷售注射用比伐蘆定的資格,。 表2:普利制藥早前已獲得的ANDA文號情況 來源:米內(nèi)網(wǎng)全球上市藥物數(shù)據(jù)庫 據(jù)米內(nèi)網(wǎng)數(shù)據(jù)顯示,早前普利制藥已獲得了7個(gè)產(chǎn)品的ANDA文號,,本次注射用比伐蘆定獲批,,有助于提升公司在美國市場的銷售業(yè)績。 來源:公司公告,、米內(nèi)網(wǎng)數(shù)據(jù)庫
來源:米內(nèi)網(wǎng)全球上市藥物數(shù)據(jù)庫 據(jù)米內(nèi)網(wǎng)數(shù)據(jù)顯示,早前普利制藥已獲得了7個(gè)產(chǎn)品的ANDA文號,,本次注射用比伐蘆定獲批,,有助于提升公司在美國市場的銷售業(yè)績。 來源:公司公告,、米內(nèi)網(wǎng)數(shù)據(jù)庫