當下的“中國”已成為全球科技界的“熱詞”之一:國際頂級學(xué)術(shù)期刊為中國科研制作特輯,;世界知識產(chǎn)權(quán)組織稱贊中國專利“井噴”,;“新四大發(fā)明”在海外“圈粉”無數(shù)……中國創(chuàng)新成為反哺全球醫(yī)藥的新動力,,世界意義更加凸顯,。特別是兩辦發(fā)布的關(guān)于深化藥品審批制度改革,,鼓勵藥品創(chuàng)新和器械創(chuàng)新意見,吹響了中國醫(yī)藥創(chuàng)新的號角,,我們迎來了醫(yī)藥創(chuàng)新的黃金時代,。
11月9日上午,秋色宜人的江蘇常州,,第29屆全國醫(yī)藥經(jīng)濟信息發(fā)布會上,,一堂關(guān)于醫(yī)藥創(chuàng)新生態(tài)變革與趨勢研判的頭腦風(fēng)暴,正在刷新著逾千名醫(yī)藥界人士對產(chǎn)業(yè)未來的認知,。CFDA南方醫(yī)藥經(jīng)濟研究所副所長,、醫(yī)藥經(jīng)濟報總編陶劍虹博士在《全球醫(yī)藥創(chuàng)新特征與中國趨勢研判》的主題報告中,首次提出了中國醫(yī)藥創(chuàng)新步入黃金時代的研判,,且讓我們隨著她共同開啟新時代的大門,,探看未來醫(yī)藥創(chuàng)新藍圖。

CFDA南方醫(yī)藥經(jīng)濟研究所副所長,、
《醫(yī)藥經(jīng)濟報》總編 陶劍虹博士
全球醫(yī)藥創(chuàng)新生態(tài)十大特點
在陶劍虹看來,,支撐中國醫(yī)藥創(chuàng)新躍升的社會環(huán)境和產(chǎn)業(yè)基礎(chǔ)已經(jīng)日臻完善。一方面,,中國醫(yī)藥衛(wèi)生事業(yè)獲得長足進展,,衛(wèi)生總費用占GDP的比重提高到6%以上,人均衛(wèi)生費用增長2倍,,醫(yī)保覆蓋率超過98%,,以臨床價值為導(dǎo)向的研發(fā)共識已經(jīng)形成。另一方面,十八大以來的五年,,我國醫(yī)藥工業(yè)規(guī)模不斷擴大,,醫(yī)藥工業(yè)總產(chǎn)值占GDP比重也從3.2%增長至4.3%。制藥百強不單追求規(guī)模擴大,,也更加關(guān)注創(chuàng)新投入,,尤其是一些創(chuàng)業(yè)型研發(fā)企業(yè)的涌現(xiàn),成為當下產(chǎn)業(yè)創(chuàng)新的活力基因,。中國式的創(chuàng)新,,融入全球產(chǎn)業(yè)變遷中,新的特點格外耐人尋味,。
| ⒈ | 全球醫(yī)藥市場增速加快,, 新興市場領(lǐng)軍新增長 |
預(yù)計2017年至2022年,世界處方藥市場將受到又一輪新藥上市潮的拉動,,保持6.5%的年均增長,,總規(guī)模到2022年將突破一萬億美元,。
過去 10 年,,全球制藥企業(yè)的研發(fā)成本增加了80%以上,而新產(chǎn)品的推出量卻減少了43%,,全球頂級戰(zhàn)略咨詢公司德國羅蘭貝格管理咨詢公司發(fā)布的《醫(yī)藥行業(yè)如何盈利》報告顯示,,被調(diào)查的企業(yè)中,75%表示他們正經(jīng)歷戰(zhàn)略危機,,而重點發(fā)展將放在高增長的新興市場,。全球醫(yī)藥經(jīng)濟的增長已經(jīng)從發(fā)達國家轉(zhuǎn)向新興市場國家。
| ⒉ | 國內(nèi)外藥審提速,, 中國企業(yè)迅速跟進FDA新批藥物 |
截至2017年10月30日,,F(xiàn)DA共批準了35個新藥,其中4個已在國內(nèi)CDE有申報,。從2016年以來,,中國新藥注冊申報量已經(jīng)占到藥品注冊申報總量的55%?;鞠怂幤纷陨暾埛e壓,,等待審評的藥品注冊申請已由2015年8月21668件降至2017年8月的3000件??股睾鸵呙缗R床試驗申請,、中藥民族藥注冊申請已實現(xiàn)按時限審評。
表1 2017年FDA新批藥物被國內(nèi)企業(yè)研發(fā)跟進情況
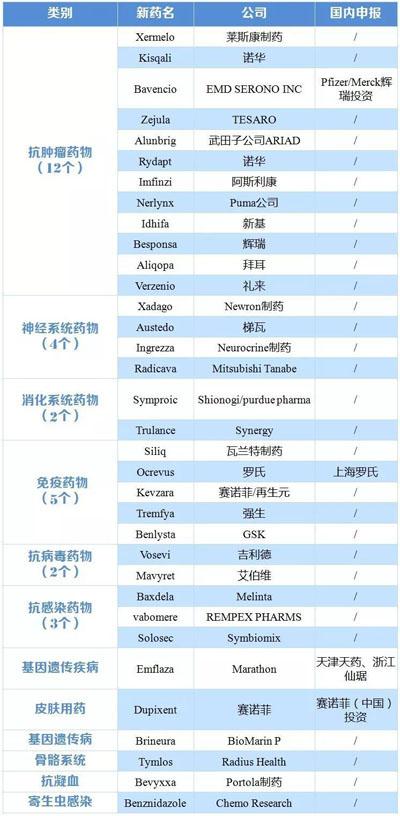
| ⒊ | 國際多中心臨床加快推開,, 中國迎來第二次進口藥浪潮 |
新制度下對進口新藥境內(nèi)上市注冊進行調(diào)整,,由原先的三報三批改為兩報兩批,進口新藥審評審批加速,2016年共批準22個,,2017年1-10月共批準51個,。截至2017年8月14日,納入優(yōu)先審評的進口受理號有144個,。進口丙肝新藥集中登陸中國,,截至目前,BMS,、強生,、吉利德、AbbVie的口服丙肝新藥已在國內(nèi)上市,,美國的丙肝市場經(jīng)歷急速爆發(fā)和迅速萎縮,,價格競爭日趨激烈,給國內(nèi)仿制企業(yè)也將帶來一定壓力,。
表2 獲得優(yōu)先審評的進口藥物及國內(nèi)企業(yè)跟進情況
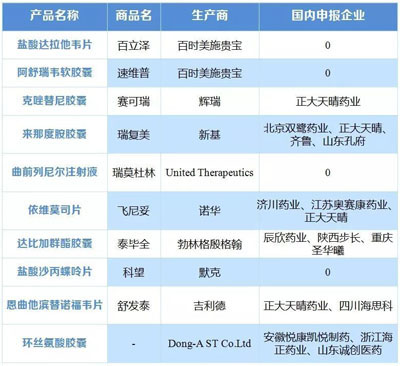
| ⒋ | 中國加入ICH開啟全球研發(fā)新格局,, 制藥巨頭持續(xù)加碼研發(fā)投入 |
2017年6月CFDA成為ICH正式成員,通過標準和指南同步,,中國的藥品審評審批標準將越發(fā)接近發(fā)達國家,。數(shù)據(jù)顯示,2017年制藥研發(fā)公司的地理分布整體向東部遷移:在華新藥研發(fā)企業(yè)數(shù)量占全球比例從4%(2016年)增長至5%(2017年),,中國已成為亞洲最大的新藥研發(fā)國,。
制藥巨頭藥企持續(xù)加碼研發(fā)投入,2017年前20強的合計銷售收入占世界藥品市場的比重為41.7%,,2017年前20強企業(yè)平均研發(fā)強度為19.6%
| ⒌ | 新藥的“買來主義”重新流行,, 大手筆并購擴充研發(fā)管線 |
由于研發(fā)的高投入、高風(fēng)險性,,近年來新藥的“買來主義”又倍受關(guān)注,。其中大型外資企業(yè)更是大刀闊行這一措施。如羅氏通過并購驅(qū)動公司發(fā)展,,其收購的藥品銷售額占總銷售額比例從2014年的77%提升至2017年的84%,。BMS通過外購潛力品種成為增速最快的公司,預(yù)計2020年將有61%的銷售額來自于收購藥品,。陶劍虹提示說:并購一般用于企業(yè)想要進入新領(lǐng)域的時候,,對于企業(yè)短期收入提升的貢獻是巨大的,也能分擔過于依賴主營研發(fā)方向的風(fēng)險,。但是企業(yè)要基業(yè)長青,,在自己主營業(yè)務(wù)上的研發(fā)投入也是必須的。羅氏能長年有如此穩(wěn)定的表現(xiàn),,就和自己多年來在腫瘤藥領(lǐng)域的持續(xù)投入分不開的,,僅2016年就有5個抗腫瘤新藥獲得FDA批準,。
表3 近年來成功擴充產(chǎn)品線的并購案例
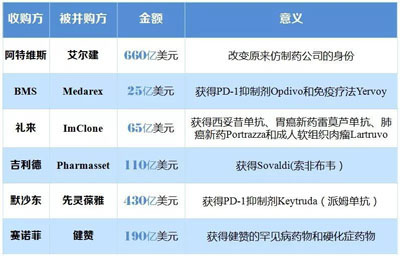
| ⒍ | 外企調(diào)整傳統(tǒng)早期研發(fā)模式, 與創(chuàng)新型小藥企合作注入新活力 |
近年,,外資藥企紛紛關(guān)閉或出售中國研發(fā)中心日漸頻繁,。其主要原因在于大型制藥企業(yè)的研發(fā)效率不高,傳統(tǒng)研發(fā)模式開始變革,,轉(zhuǎn)而與研發(fā)效率更高的早期研發(fā)型小企業(yè)合作,。在中國,創(chuàng)新藥企與國外藥企交易合作也逐漸增多,,2000年到2016年,,中國藥企對外交易合作年平均增長率為19%。
表4 中國藥企與國外藥企重磅交易TOP 10(億美元)
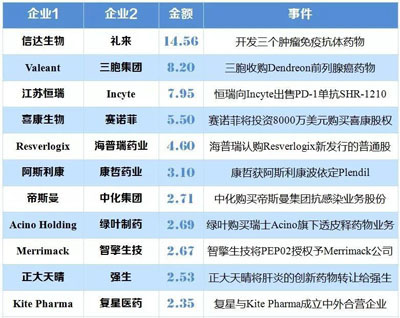
| ⒎ | MAH銜接初創(chuàng)企業(yè)與制藥業(yè),, 全球醫(yī)藥外包需求上漲 |
目前,,全球前10的大藥廠基本都是外部購買創(chuàng)新早期項目、進行后期開發(fā)為主,。在中國,,制藥前50大企業(yè),也紛紛涉足創(chuàng)新藥領(lǐng)域?,F(xiàn)階段,,中國實施的上市許可人制度(MAH)推動初創(chuàng)企業(yè)與制藥企業(yè)的協(xié)同創(chuàng)新。如BGB-A317注射液,,申請人和持有人是百濟神州,,受委托企業(yè)為勃林格殷格翰生物藥業(yè)(中國)。華領(lǐng)醫(yī)藥的HMS5552及其片劑,,其受委托企業(yè)為合全藥業(yè)、迪賽諾生物醫(yī)藥,。國內(nèi)CMO/CDMO市場由2011年的18億美元增長至今年的50億美元,,復(fù)合增速達到18.6%。預(yù)計到2020年,,國內(nèi)市場規(guī)模將達到85億美元,,約占全球市場比重的9.7%。
| ⒏ | 仿制藥行業(yè)降價壓力增大,, “突破性”仿制藥加快上市進程 |
仿制藥將繼續(xù)面臨降價壓力,,以梯瓦為例,其股價在2017年8月下跌24%,,其核心產(chǎn)品多發(fā)性硬化癥藥物格拉替雷面臨專利挑戰(zhàn),,很可能因此失去獨家產(chǎn)品地位,此外梯瓦還受到同類競品Tecfidera的有力競爭,。特朗普政府多次抨擊藥品價格過高,,F(xiàn)DA開始大大加快仿制藥審批,優(yōu)先接受超過100種突破性仿制藥的申請,這一舉措增強了市場競爭,,同時也降低了藥品價格,,預(yù)測2017年底美國仿制藥平均降價9%。
陶劍虹著重指出,,CDE公布了首批專利過期還沒有仿制藥品的目錄,,在激發(fā)創(chuàng)新活力的同時,國內(nèi)適合型藥企可以作參考,。
表5 首批專利權(quán)到期,、終止、無效尚且無仿制申請的藥品清單
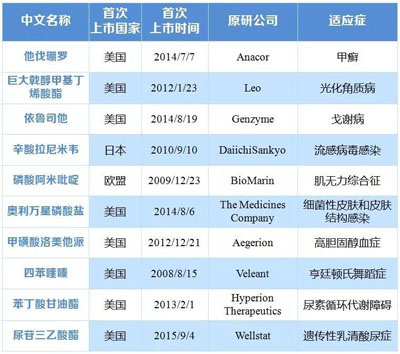
| ⒐ | 生物仿制藥市場方興未艾,, 中國在研產(chǎn)品數(shù)量領(lǐng)先 |
目前在世界范圍內(nèi),,有近850種生物仿制藥開發(fā)或銷售,其中約125個在臨床試驗,。有超過515種改良型生物仿制藥開發(fā)或銷售,,其中200多個在臨床試驗。大約五年內(nèi),,生物仿制藥將超過其他創(chuàng)新產(chǎn)品,。目前,在研生物類似藥的主要分布地區(qū)排名第一的是中國大陸,,美國位居第三,。一方面反映了中國巨大的市場需求,也反映了中國生物類似藥的激烈競爭,。
全世界有80%的在研生物類似藥的適應(yīng)癥是自身免疫病和腫瘤相關(guān)疾病,不論是中國還是從全球,,單抗占在研生物類似藥的比例都是最高的,中國達到40.7%,。目前,,國內(nèi)不少藥企都在生物類似藥上布局。據(jù)湯森路透的報道,,2016年蘇州康寧杰瑞在研生物類似藥的數(shù)目已有28個之多,,其次,齊魯制藥在研生物類似藥數(shù)量也達到10個,。
2016年全球藥品銷售額Top10中6款單抗藥分別為:貝伐珠單抗,、阿達木單抗、曲妥珠單抗,、利妥昔單抗,、英夫利西單抗和依那西普單抗。其專利在歐盟和美國即將到期(部分在歐盟于2015年和2017年專利已到期),。目前這6款單抗在我國均已有在研企業(yè),,貝伐珠單抗類似藥在研企業(yè)共14家,、阿達木單抗類似藥在研企業(yè)共15家、曲妥珠單抗類似藥在研企業(yè)共13家,、利妥昔單抗類似藥在研企業(yè)共6家,、英夫利西單抗類似藥在研企業(yè)共3家、依那西普單抗類似藥在研企業(yè)共7家,。
| ⒑ | 孤兒藥研發(fā)迎合臨床價值導(dǎo)向,, 中國罕見病用藥迎來政策利好 |
現(xiàn)階段全球超過6000種罕見病,獲批的孤兒藥僅有400多個,,罕見病用藥缺口較大,。陶劍虹分析說,孤兒藥研發(fā)的具有自身優(yōu)勢,,一是所需病人較少,,不少在二期臨床完成后就可以上市。二是孤兒藥研發(fā)的成功率三倍于一般藥物研發(fā),。三是上市后的商業(yè)推廣費用低,,加上7-10年的獨占期,使其他仿制藥廠無法跟隨,。四是孤兒藥在上市后可以拓展新的適應(yīng)癥,,商業(yè)價值很大,易變?yōu)橹匕醍a(chǎn)品,。
據(jù)預(yù)算,,全球孤兒藥的銷售總額在2022年將達2090億美元。中國2017年也將通過發(fā)布罕見病目錄,、優(yōu)先審評審批,、條件性允許境外新藥上市以及醫(yī)保準入等加速孤兒藥研發(fā)上市。開放孤兒藥將是國內(nèi)企業(yè)值得關(guān)注的領(lǐng)域,。
小結(jié)
醫(yī)藥創(chuàng)新進入黃金時代
陶劍虹在梳理了全球醫(yī)藥創(chuàng)新生態(tài)十大特征之后,,指出:中國醫(yī)藥創(chuàng)新正步入黃金時代,這個內(nèi)涵具體包括:
伴隨著未來人口老齡化,、居住城市化、人們健康意識增強以及疾病譜變化,,促使醫(yī)藥需求持續(xù)增長,。未來5-10年是醫(yī)藥發(fā)展的關(guān)鍵時期,也是大有可為的戰(zhàn)略機遇期,。
未來醫(yī)藥研發(fā)將進一步發(fā)生價值鏈重構(gòu),,資源全球配置。從實驗室到臨床研,,從藥企到研發(fā)外包,,從資本孵化到上市,,需要形成多方融合的創(chuàng)新生態(tài)系統(tǒng)。故新藥的“買來主義”重新流行,,大手筆并購擴充研發(fā)管線,。
鑒于仿制藥特征,“突破性”仿制藥加快上市進程,,生物類似藥大品種市場方興未艾,,中國市場通過“質(zhì)量和療效一致性”的仿制藥將成主流。
中國加入ICH將開啟全球研發(fā)新格局,,研發(fā)投入持續(xù)加碼,,國內(nèi)外藥審提速,新藥上市加快以滿足臨床需求,。
中小型生物醫(yī)藥公司的崛起,,致使某些大型藥企調(diào)整傳統(tǒng)早期研發(fā)模式,與專注研發(fā)型公司注資委托授權(quán)合作,。
與國際主流對比,,差距與挑戰(zhàn)依然存在,中國將迎來第二次進口藥品熱潮,,市場競爭會變得愈發(fā)激烈,,進口替代,超越競爭的新模式隨之而生,,在競爭中成長和成熟,。
聚焦凸顯臨床價值三大品類
抗腫瘤用藥:
免疫療法異軍突起
全球腫瘤藥市場預(yù)計達1500億美元,預(yù)測腫瘤藥花費到2020年的年增長率為7.5%-10.5%,。從全球不同地區(qū)的抗腫瘤市場來看,,美國最大,其次是歐盟和日本市場,,含中國在內(nèi)的新興市場則保持逐年擴增,。在中國醫(yī)院用藥市場,抗腫瘤藥物的銷售規(guī)模近幾年來穩(wěn)步增長,,2016年中國腫瘤藥市場銷售1069億元,,增長10.2%。
研發(fā)進展來看,,2017年1-10月FDA批準上市的抗腫瘤藥有12個,,國內(nèi)批臨床的抗腫瘤1類新藥(15個)。現(xiàn)階段PD1/PDL1市場增長迅速,,2016年市場份額約60億美元,。該類原研藥也逐漸進入我國市場,與此同時,,研發(fā)繼續(xù)呈現(xiàn)火熱,。
表6 國內(nèi)企業(yè)申報的PD1/PD-L1藥物及研發(fā)階段
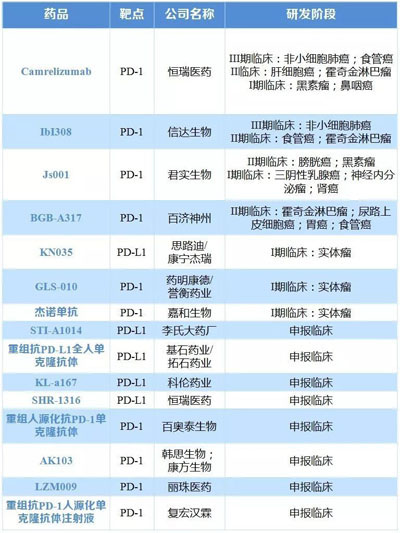
腫瘤的CAR-T療法讓腫瘤治療進入嶄新時代,,美國是CAR-T療法的發(fā)源地,不僅上市了首款CAR-T療法,,其臨床試驗進行數(shù)量也遙遙領(lǐng)先(97項),。中國已躋身CART研發(fā)第一團隊,以66項臨床試驗數(shù)量位居第二,,目前國內(nèi)已有多家企業(yè)CAR-T 研發(fā)項目推進至臨床階段,。未來CAR-T全球血液腫瘤市場有望達117 億美元,國內(nèi)血液腫瘤市場有望達111億元,。
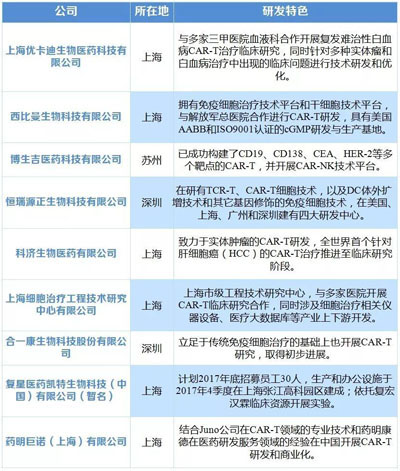
表7 國內(nèi)多家企業(yè)正在進行 CAR-T 研發(fā)
降血脂用藥:
PCSK9抑制劑方興未艾
降血脂用藥醫(yī)院銷售集中度較高,,他汀類制劑占降血脂用藥91.8%,以外企為主,,阿托伐他汀和瑞舒伐他汀合計占了整個他汀類僅8成市場,。
PCSK9 抑制劑是“后立普妥時代”最強大的降脂新藥,2015年7月24日FDA首個批準上市的PCSK9抑制劑商品名為Praluent(通用名:阿利庫單抗),,原研廠家是賽諾菲/再生元,;歐盟首個上市的PCSK9抑制劑是在2015年7月22日,商品名為:Repatha(通用名:依伏庫單抗),,原研廠家是安進,,同年8月27日獲得美國FDA批準。安進的依伏庫單抗已于2015年9月在中國獲得臨床批件,,賽諾菲/再生元的阿利庫單抗也于2015年12月獲得臨床批件,,目前都在我國進行國際多中心Ⅲ期臨床研究,國內(nèi)同類品種西威埃的CVI-LM001片已于2016年3月拿到臨床批件,,君實生物的PCSK9單抗注射液在2017年7月拿到臨床批件,。
糖尿病用藥:
胰島素長盛不衰
到2040年,糖尿病相關(guān)醫(yī)療費用將突破8020億美元,。目前,,糖尿病用藥已躍居全球藥品銷售排行第二位,僅次于腫瘤用藥,。根據(jù)IMS 統(tǒng)計,,2015 年全球糖尿病藥物市場中,胰島素產(chǎn)品約占56%,、GLP-1 受體激動劑類藥物約占10%,、DPP-4 抑制劑類藥物占24%、SGLT-2 抑制類藥物占5%,、其他傳統(tǒng)小分子降糖藥占4%。
我國口服糖尿病用藥中,,列汀類屬DPP4抑制劑,,是近年來較受關(guān)注的分支領(lǐng)域,,現(xiàn)臨床基本為外企產(chǎn)品。國內(nèi)多家企業(yè)已紛紛進行研發(fā),,如江蘇恒瑞的瑞格列汀,、江蘇豪森的貝格列汀、山東綠葉的艾格列汀等等,,均在申報中,,未來會有較多相關(guān)產(chǎn)品獲批上市;格列奈類在臨床上現(xiàn)僅有三個品種,,國內(nèi)企業(yè)競爭力在不斷提升,。
醫(yī)藥產(chǎn)業(yè)未來研判十大趨勢
陶劍虹對醫(yī)藥創(chuàng)新從宏觀到微觀的分析,吸引了與會代表的極大關(guān)注,,她對中國醫(yī)藥產(chǎn)業(yè)未來十大趨勢的研判,,進一步揭示了一個創(chuàng)新年代的活力圖景。陶劍虹指出,,隨著云計算,、物聯(lián)網(wǎng)、大數(shù)據(jù),、人工智能等新技術(shù)登上舞臺,,中國已經(jīng)站在了第四次產(chǎn)業(yè)崛起領(lǐng)跑者的位置上。新一輪技術(shù)變革的核心是智能化與信息化,。消費升級觸發(fā)上游裂變,,以智能化為核心的新制造,以O(shè)+O為路徑的新零售,,在融合中催化中國醫(yī)藥經(jīng)濟的重構(gòu)升級,。
互聯(lián)網(wǎng)+大健康,新實業(yè)+新技術(shù),,新制造+新零售,,傳統(tǒng)與新銳、科技與人文,、智能與匠心,,正在變革中共振,拓展著中國醫(yī)藥產(chǎn)業(yè)的向上空間,!
在2017年的深秋,,我們不難感受到下一個暖春的氣息,如何在下一輪周期波動中拐點向上,,政策紅利與轉(zhuǎn)型壓力,,考驗著中國醫(yī)藥經(jīng)濟的韌性,而日益活躍的創(chuàng)新平臺與資本流量,,為產(chǎn)業(yè)發(fā)展增添了張力,。具體表現(xiàn)在:
1
消費升級是值得期待的風(fēng)口
消費逐漸成為經(jīng)濟增長的第一驅(qū)動力,,2016年最終消費對經(jīng)濟增長貢獻率達到 64.6%,未來提升空間仍然巨大,。最近十年大量的醫(yī)保投入和居民收入的增加,,使得“因病致貧”已經(jīng)大量減少,腫瘤從治療角度,,心腦血管從早期預(yù)防與治療角度已經(jīng)有很大改觀,,未來市場需求將繼續(xù)提升。同時消費升級使得??朴盟幨袌鍪芤?,專科藥物就診量小,,藥品利潤高,,例如:類風(fēng)濕在我國發(fā)病人群每年在500萬以上,屬于不死的癌癥,,在發(fā)達國家治療概率非常高,,而在國內(nèi)治療率也僅僅在10% ,還有很大的成長空間,。
2
VR和AI會刷新研發(fā)效率
越來越多的高科技被藥企應(yīng)用于新藥研發(fā)領(lǐng)域,,借此探索提高新藥研發(fā)效率、節(jié)省更多成本的路徑,,如:應(yīng)用于藥物研發(fā)項目的輝瑞365平臺上描述的VR系統(tǒng)名為輔助虛擬環(huán)境(CAVE),,用投影儀打造虛擬現(xiàn)實場景,讓研究人員更快捷的探索數(shù)據(jù),。強生倫敦創(chuàng)新中心將一些處于試驗中的小分子化合物轉(zhuǎn)交給了BenevolentAI公司進行開發(fā),,利用人工智能系統(tǒng)來指導(dǎo)臨床試驗的進行和數(shù)據(jù)的收集。日本的鹽野義制藥等近50家日本企業(yè)將參加利用人工智能推進新藥開發(fā)的項目,。
3
醫(yī)藥新實業(yè)轉(zhuǎn)型重塑
醫(yī)藥新實業(yè)的轉(zhuǎn)型需提高三大能力:整合營銷能力,、供應(yīng)鏈能力、金融資本能力,。同時,,制藥工業(yè)與工業(yè)4.0逐步融合。“工業(yè)4.0”使制造業(yè)模式可以從傳統(tǒng)的以產(chǎn)品為中心向以用戶為中心轉(zhuǎn)變,,其中包括生產(chǎn)模式從大規(guī)模流水線生產(chǎn)轉(zhuǎn)向定制化規(guī)模生產(chǎn)轉(zhuǎn)變,。但是由于制藥行業(yè)產(chǎn)品(藥品)的特殊性,一般不可能依據(jù)消費者(患者)的喜好來定制化生產(chǎn),。不過,,制藥裝備就可以有定制化的需求,尤其3D打印技術(shù)在醫(yī)藥領(lǐng)域的運用發(fā)展較快。
4
供應(yīng)鏈創(chuàng)新促醫(yī)藥流通升級
2017年10月,,國務(wù)院辦公廳印發(fā)《關(guān)于積極推進供應(yīng)鏈創(chuàng)新與應(yīng)用的指導(dǎo)意見》,,指出“推動流通創(chuàng)新轉(zhuǎn)型、推進流通與生產(chǎn)深度融合和提升供應(yīng)鏈服務(wù)水平”,。為例藥品流通企業(yè)利用物聯(lián)網(wǎng)、區(qū)塊鏈等技術(shù),,建設(shè)供應(yīng)鏈一體化管理平臺,,打通物流、資金流和信息流的隔閡,;向供應(yīng)鏈上下游提供市場開發(fā),、價格談判、在線支付,、金融支持等增值服務(wù)及綜合解決方案,,借助云計算、大數(shù)據(jù)等技術(shù)挖掘數(shù)據(jù)的價值,,輔助企業(yè)及終端客戶的經(jīng)營決策,,從根本上解決信息孤島問題。
5
O+O全渠道開啟醫(yī)藥新零售時代
信息技術(shù)的充分發(fā)展為新零售提供強大保障,,電商巨頭借助信息技術(shù)實現(xiàn)消費者為中心的線上線下數(shù)據(jù)全面打通已經(jīng)成為可能,,也為新零售模式下以消費者為中心重構(gòu)人、貨,、場提供強大保障,。由此,醫(yī)藥O+O將會逐漸成為中國零售藥店轉(zhuǎn)型的主流選擇,。
隨著處方外流加速,,國內(nèi)DTP藥房將迎來發(fā)展良機。預(yù)計到2020年,,DTP的市場容量將接近400億元,。隨著創(chuàng)新藥加速上市,慢病和腫瘤等自費治療性用藥比例提升,,DTP藥房逐步由經(jīng)營新特藥向?qū),?扑幯葑儯瑢{借其專業(yè)的用藥咨詢服務(wù)等優(yōu)勢,,成為處方外流的主要承接方之一,。
6
工商企業(yè)大融合時代到來
陶劍虹把上游工業(yè)企業(yè),按照科技含量和產(chǎn)品價格的維度,,切出了五類的醫(yī)藥企業(yè),,分別是2000家到3000家僵尸企業(yè)、低成本高質(zhì)量的加工能力強的生產(chǎn)企業(yè)、有獨特產(chǎn)品的特異性中小型企業(yè),、綜合性大型企業(yè) ,、大型外企。這五類醫(yī)藥企業(yè)里面其實都已經(jīng)完成了自己的定位,。中國企業(yè)戰(zhàn)略資源的配置是重視營銷和生產(chǎn)的配置,,而國際大中型企業(yè)典型資源配置是重視研發(fā)和營銷的配置。兩票制,、營改增的時代,,是工商企業(yè)高度融合的時代!戰(zhàn)略理念的契合匹配是持續(xù)發(fā)展走的更遠的基礎(chǔ),。邊界正在消失,,研發(fā)和營銷可以是一體的,一個有創(chuàng)新力的企業(yè)一定是富有營銷活力的企業(yè),!
7
研發(fā)創(chuàng)新產(chǎn)業(yè)集群形成,,灣區(qū)經(jīng)濟將凸顯
在全球范圍內(nèi)醫(yī)藥研發(fā)產(chǎn)業(yè)集群正在逐步形成和聚合。灣區(qū)經(jīng)濟作為重要的濱海經(jīng)濟形態(tài),,是當今國際經(jīng)濟版圖的突出亮點,,是世界一流濱海城市的顯著標志。2017年 “粵港澳大灣區(qū)”首次出現(xiàn)在《政府工作報告》,。相比紐約灣區(qū),、東京灣區(qū)、舊金山灣區(qū)等世界著名的幾大灣區(qū),,粵港澳大灣區(qū)的GDP總量還不夠大,,人均GDP更少,梯度差異仍然明顯,?;浉郯拇鬄硡^(qū)將成為新的驅(qū)動發(fā)展模式、改革開放的升級版,。
8
高性能醫(yī)療器械產(chǎn)業(yè)發(fā)展圖景逐漸清晰
《中國制造2025 重點領(lǐng)域技術(shù)路線圖》提出到2030 年我國醫(yī)療器械產(chǎn)業(yè)規(guī)模要達到3 萬億并完成1 萬億的出口目標,,則未來15 年該行業(yè)至少將保持約16.39%的復(fù)合增速。我國醫(yī)療器械消費占比遠低于國際平均水平,,具有廣闊的成長空間,。預(yù)計在國家對醫(yī)療器械國產(chǎn)化政策的大力推動下,高端國產(chǎn)醫(yī)療器械將獲得長足發(fā)展,?;鶎雍头枪⑨t(yī)療機構(gòu)的醫(yī)療器械市場空間廣闊,家用醫(yī)療器械市場預(yù)計也將快速增長,。
9
中國大健康產(chǎn)業(yè)蓬勃發(fā)展
美國健康產(chǎn)業(yè)是近十年來增速最快的產(chǎn)業(yè),,占GDP的比重為8.8%,。中國大健康產(chǎn)業(yè)占GDP的比重為5.6%。陶劍虹指出:和美國相比,,中國的大健康產(chǎn)業(yè)處于初創(chuàng)期,,醫(yī)藥產(chǎn)業(yè)尤其是醫(yī)藥制造部分的占比很重,健康服務(wù)產(chǎn)業(yè)發(fā)展還有很大空間,,在產(chǎn)業(yè)細分以及結(jié)構(gòu)合理化方面需要更大的提升和完善,。
特醫(yī)食品是大健康產(chǎn)業(yè)的下一場盛宴?!短厥忉t(yī)學(xué)用途配方食品注冊管理辦法》 2016年7月1日正式實施,,海外特醫(yī)食品巨頭、國內(nèi)企業(yè)尤其是制藥企業(yè)躍躍欲試,,特醫(yī)食品迎來了其發(fā)展的新機遇。隨著中國社會老齡化加速,,中國特醫(yī)食品未來的市場規(guī)模將超過100億元,。
10
“健康中國”帶動醫(yī)養(yǎng)結(jié)合快速發(fā)展
陶劍虹在最后指出,令人倍感振奮的是,,十九大報告提出“健康中國”戰(zhàn)略,。明確了人民健康是民族昌盛和國家富強的重要標志。“大健康”理念將從理論付諸實踐,、醫(yī)療衛(wèi)生體制改革將全面破解世界難題,、從田野到餐桌的食品安全防線將全面構(gòu)建,為全體國民描繪“健康中國”的實施路線圖,。未來,,國家將積極應(yīng)對人口老齡化,構(gòu)建養(yǎng)老,、孝老,、敬老政策體系和社會環(huán)境,推進醫(yī)養(yǎng)結(jié)合,,加快老齡事業(yè)和產(chǎn)業(yè)發(fā)展,。智慧養(yǎng)老將是醫(yī)藥企業(yè)值得關(guān)注的跨界整合領(lǐng)域。
重拾創(chuàng)新初心的“漂亮”哲學(xué)
陶劍虹如此全景式的展望中國醫(yī)藥產(chǎn)業(yè)的廣闊前景,,令醫(yī)藥人心潮起伏,,但她同樣也提示大家直面中國醫(yī)藥創(chuàng)新的冷峻現(xiàn)實。創(chuàng)新沒有完美的終點,,需要在壓力下優(yōu)雅前行,。創(chuàng)新需要外部的激勵,更需要參與創(chuàng)新的人不斷給自己激勵,。陶劍虹娓娓道來:“關(guān)于這一點,,我想說兩個有趣的故事,,傳說蝸牛從前是沒有殼的,但他爬到上蒼那里去,,祈求上蒼賜給它一個殼,。 為什么一定要裝美麗的殼呢?虛偽還是自欺欺人,? 蝸牛沉思片刻,,鄭重回答:為了僅此一次的生命。在激烈的市場競爭中,,中國企業(yè)還沒有自信承受多次的研發(fā)失敗,,因為太多的不確定性讓企業(yè)沒有足夠的定力,為了創(chuàng)新僅此一次的生命,,讓我們給新藥研發(fā)更好的孵化器,,讓脆弱的藥物創(chuàng)新受到多一些保護。”
在陶劍虹看來,,創(chuàng)新這條路并不歡迎悲情英雄,,新藥研發(fā)的探索者要有一種牽著蝸牛散步的豁達。借用“反脆弱”的理念,,就是要勤于實驗,,廣泛播種,著眼長期,,靈活轉(zhuǎn)向,,簡勝于繁,總結(jié)反思,。
而她援引的另一個故事描述的是原本善于飛翔的蝸牛獲得飛行比賽的冠軍之后,,不思進取,自我陶醉,,結(jié)果翅膀退化,,獎杯成了堅硬的外殼,只能在地上爬行,。她意味深長地說:“這是一個警醒,,即使在研發(fā)的道路上你已經(jīng)走得很遠,也不能忘記當初為何出發(fā),。既然選擇了遠方,,便只顧風(fēng)雨兼程;我們只需確定,,守住最初的浪漫,,要贏就贏得漂亮。”
■本報記者 董菊紅
■編輯 陳麗
當前頁面地址:http://www.zgysw.net/news/3851.html



