主動免疫療法為通過腫瘤抗原刺激患者自身免疫系統(tǒng)產(chǎn)生特異性免疫應(yīng)答從而殺傷腫瘤細(xì)胞,。在多種惡性實(shí)體腫瘤如胰腺癌中,主動免疫療法已獲得顯著療效,。有研究表明,,在膠質(zhì)母細(xì)胞瘤(GBM)內(nèi)和周圍腦實(shí)質(zhì)中存在CD8陽性T細(xì)胞。由于GBM可能減少M(fèi)HC表達(dá)和抗原遞呈,,以及后續(xù)化療的影響導(dǎo)致免疫逃逸,,從而機(jī)體無法通過免疫系統(tǒng)殺傷GBM腫瘤細(xì)胞。
荷蘭,、比利時以及美國的科學(xué)家將手術(shù)獲得的腫瘤細(xì)胞制成疫苗,,并使用粒細(xì)胞-巨噬細(xì)胞集落刺激因子(GM-CSF)加強(qiáng)樹突狀細(xì)胞遞呈抗原的能力,可以顯著地提高免疫療法在復(fù)發(fā)GBM中的治療效果,,臨床結(jié)果發(fā)表在2015年5月的《Vaccine》雜志上,。
作者提出的免疫治療方案稱為Gliovac療法(glioma vaccine)。手術(shù)獲得無菌的GBM腫瘤組織,,經(jīng)排除血液傳播疾病后立即送入實(shí)驗(yàn)室。先機(jī)械分離細(xì)胞,,然后使用厄爾平衡鹽緩沖液(EBSS)洗滌,,接著細(xì)胞計數(shù),并使用DNFB處理,以增加抗原性,。將這些細(xì)胞等分成兩份后,,一份細(xì)胞凍存于蔗糖中,另一份則使用滲透壓沖擊方法裂解,。以上兩份再經(jīng)過25Gy伽馬射線照射破壞DNA,,使其不再具有增殖活性。經(jīng)過以上處理后,,所有疫苗保存在-80℃環(huán)境中,。
患者術(shù)后第十天開始接受第一個Gliovac療程,先口服3天小劑量環(huán)磷酰胺以減少抑制性免疫細(xì)胞,,然后分5次進(jìn)行疫苗(細(xì)胞+裂解物)和GM-CSF皮下注射,,其中2次注射患者自體同源疫苗,,另3次分別使用來源于其他3例GBM患者的同種異源疫苗。每28天為1療程,,共進(jìn)行6個療程治療(圖1),。
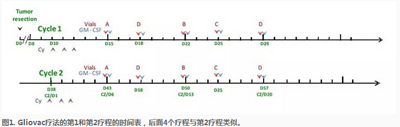
臨床試驗(yàn)前的動物實(shí)驗(yàn)提示,采用Gliovac方案(環(huán)磷酰胺+疫苗+GM-CSF)比單用疫苗,、或單用環(huán)磷酰胺,、或環(huán)磷酰胺+GM-CSF、或環(huán)磷酰胺+疫苗等方案相比可以顯著減少大鼠模型(CNS-1 Lewis)的腫瘤體積,。在動物實(shí)驗(yàn)的基礎(chǔ)上,,荷蘭、比利時和美國于2012年至2014年間開展臨床研究,,納入9例經(jīng)過手術(shù)+TMZ同步放化療和部分接受過貝伐單抗等標(biāo)準(zhǔn)治療的復(fù)發(fā)GBM患者,,其中5例女性,4例男性,;年齡27歲~63歲,; KPS平均80分。
如果不進(jìn)一步治療,,9例患者的預(yù)期生存時間在1個月至4.5個月之間,,因此患者均愿意接受再次手術(shù)和術(shù)后免疫治療。臨床研究以嚴(yán)重不良反應(yīng)作為主要終點(diǎn),,以中位總生存期和影像學(xué)表現(xiàn)作為次要終點(diǎn),。
免疫治療后隨訪發(fā)現(xiàn),所有患者的不良反應(yīng)短暫且輕微,,2例頭痛,,4例注射部位出現(xiàn)紅斑。局部的皮膚反應(yīng)是一種機(jī)體免疫的應(yīng)答表現(xiàn),,與療效之間不存在明顯關(guān)系,。
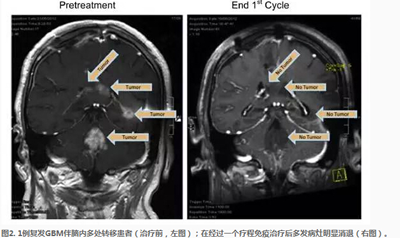
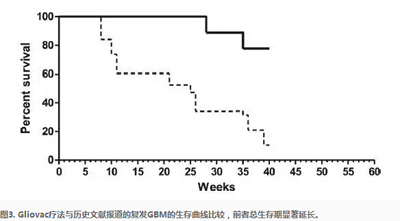
使用RANO標(biāo)準(zhǔn)評價腫瘤治療后的影像學(xué)表現(xiàn),發(fā)現(xiàn)多數(shù)患者的殘留腫瘤顯著消退(圖2),。與以前文獻(xiàn)發(fā)表的復(fù)發(fā)膠質(zhì)瘤生存期相比,,Gliovac療法顯著延長患者總生存期,40周比10周(圖3),。
以上結(jié)果顯示,,Gliovac療法的安全性和效果都是令人矚目的,目前美國FDA已經(jīng)批準(zhǔn)開展Ⅱ期臨床研究,,注冊號為NCT1903330,。
目前已經(jīng)登錄國內(nèi)專利
更多信息請關(guān)注:醫(yī)旅在線

當(dāng)前頁面地址:http://www.zgysw.net/news/4317.html



