《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范(2014版)》(以下簡(jiǎn)稱(chēng)《規(guī)范》)標(biāo)志著醫(yī)療器械生產(chǎn)行業(yè)最嚴(yán)監(jiān)管時(shí)代的來(lái)臨,。 國(guó)家食藥監(jiān)管總局要求,從2016年1月1日起所有第三類(lèi)醫(yī)療器械生產(chǎn)企業(yè)必須符合《規(guī)范》要求,,其他醫(yī)療器械生產(chǎn)企業(yè)應(yīng)于2018年1月1日符合《規(guī)范》要求,。 今年春年前后,國(guó)家局下發(fā)通知,,要求各地食藥監(jiān)管部門(mén)針對(duì)第三類(lèi)醫(yī)療器械生產(chǎn)企業(yè)開(kāi)展督查,。廣東、安徽,、浙江三省已開(kāi)先河,,不少械企被限期整改、停產(chǎn)整改,,乃至注銷(xiāo),。相關(guān)情況,中國(guó)醫(yī)療器械近期都有報(bào)道,。 問(wèn)題來(lái)了,,史上最嚴(yán)監(jiān)管究竟是如何具體實(shí)施的? 據(jù)悉,,安徽省食藥監(jiān)局近日出臺(tái)的《關(guān)于監(jiān)督實(shí)施醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范的意見(jiàn)》規(guī)定,,在日常監(jiān)督檢查中,只要發(fā)現(xiàn)企業(yè)一般項(xiàng)目不符合要求的,,一律責(zé)令企業(yè)限期整改,;若是關(guān)鍵項(xiàng)目不符合要求,或者雖僅有一般項(xiàng)目不符合要求但會(huì)對(duì)產(chǎn)品質(zhì)量產(chǎn)生直接影響的,,企業(yè)必須停產(chǎn)整改,;情節(jié)嚴(yán)重的,,或?qū)⒅苯颖坏蹁N(xiāo)生產(chǎn)許可證,。 從中不難看出,關(guān)鍵項(xiàng)目不合要求就停產(chǎn)整改,,可謂一拳定生死,。而停產(chǎn)對(duì)企業(yè)的災(zāi)難性影響則是不言而喻。 那么,會(huì)導(dǎo)致企業(yè)停產(chǎn)的“關(guān)鍵項(xiàng)目”都有啥,? 去年10月,,國(guó)家局在其官網(wǎng)上發(fā)布了4份現(xiàn)場(chǎng)檢查指導(dǎo)原則,包括一個(gè)總的原則,,以及三種具體類(lèi)型的原則(無(wú)菌,、植入性醫(yī)療器械和體外診斷試劑)。 中國(guó)醫(yī)療器械將其中的關(guān)鍵項(xiàng)目匯總?cè)缦?,共?jì)57項(xiàng): 1,、機(jī)構(gòu)和人員,計(jì)5項(xiàng)  備注:未經(jīng)特殊說(shuō)明的均為共有關(guān)鍵項(xiàng)目,,各類(lèi)型企業(yè)均需遵守的,,以下同。 2,、廠(chǎng)房與設(shè)施,,計(jì)8項(xiàng)
備注:未經(jīng)特殊說(shuō)明的均為共有關(guān)鍵項(xiàng)目,,各類(lèi)型企業(yè)均需遵守的,,以下同。 2,、廠(chǎng)房與設(shè)施,,計(jì)8項(xiàng) 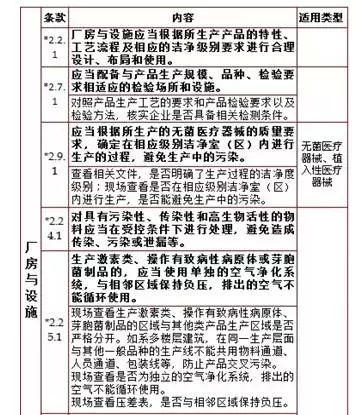
 3、設(shè)備,,計(jì)3項(xiàng)
3、設(shè)備,,計(jì)3項(xiàng) 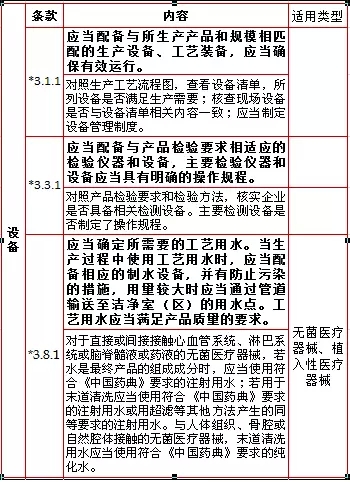 4,、文件管理,計(jì)2項(xiàng)
4,、文件管理,計(jì)2項(xiàng)  5,、設(shè)計(jì)開(kāi)發(fā),,計(jì)2項(xiàng)
5,、設(shè)計(jì)開(kāi)發(fā),,計(jì)2項(xiàng) 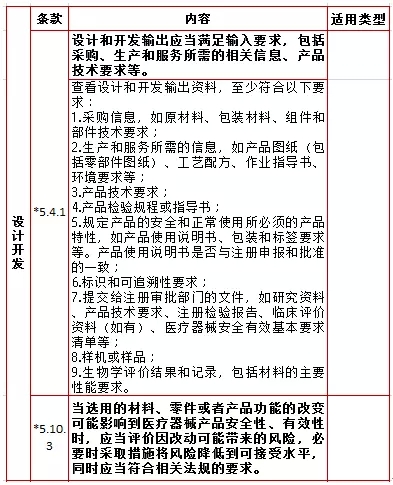 6、采購(gòu),,計(jì)12項(xiàng)
6、采購(gòu),,計(jì)12項(xiàng) 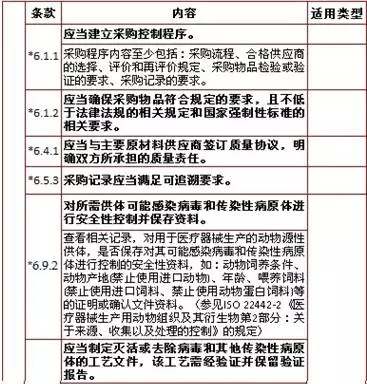

 7,、生產(chǎn)管理,計(jì)11項(xiàng)
7,、生產(chǎn)管理,計(jì)11項(xiàng) 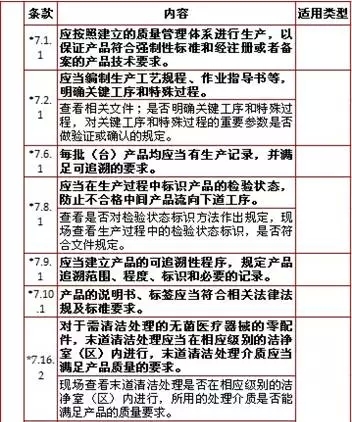
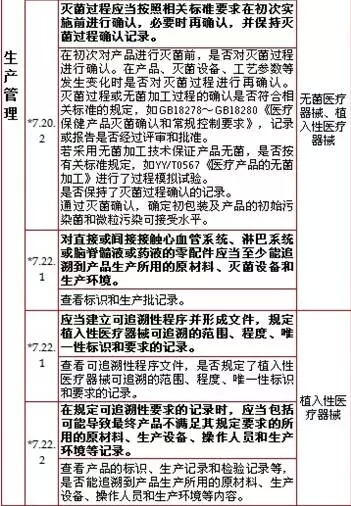 8,、質(zhì)量控制,,計(jì)8項(xiàng)
8,、質(zhì)量控制,,計(jì)8項(xiàng) 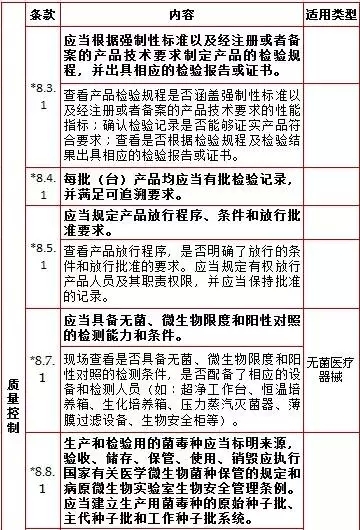
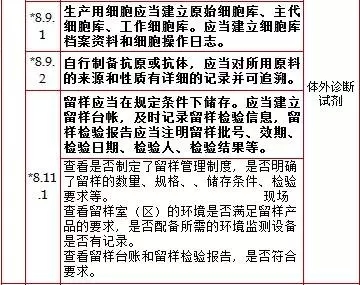 9、銷(xiāo)售和售后服務(wù),,計(jì)1項(xiàng) *9.1.1 應(yīng)當(dāng)建立產(chǎn)品銷(xiāo)售記錄,,并滿(mǎn)足可追溯要求。 10,、不合格品控制,,計(jì)1項(xiàng)
9、銷(xiāo)售和售后服務(wù),,計(jì)1項(xiàng) *9.1.1 應(yīng)當(dāng)建立產(chǎn)品銷(xiāo)售記錄,,并滿(mǎn)足可追溯要求。 10,、不合格品控制,,計(jì)1項(xiàng)  11、不良事件監(jiān)測(cè),、分析和改進(jìn),,計(jì)4項(xiàng)
11、不良事件監(jiān)測(cè),、分析和改進(jìn),,計(jì)4項(xiàng)  經(jīng)過(guò)梳理,中國(guó)醫(yī)療器械發(fā)現(xiàn),,此次督查不可不謂時(shí)間緊,、任務(wù)重,、動(dòng)真格。 比如安徽省要求在今年6月底前就完成所有第三類(lèi)醫(yī)療器械生產(chǎn)企業(yè)質(zhì)量管理體系的全面檢查,。而浙江全省236家第三類(lèi)醫(yī)療器械生產(chǎn)企業(yè)中,,已有20家被限期整改,6家被停產(chǎn)整改,,還有4家主動(dòng)停產(chǎn),,1家注銷(xiāo)等等,占比近15%,。預(yù)測(cè)日后會(huì)有更多省份陸續(xù)展開(kāi)相關(guān)督查工作,,新一輪督查風(fēng)暴即將來(lái)襲! 此外,,國(guó)家局要求,,第三類(lèi)以外的其他醫(yī)療器械生產(chǎn)企業(yè)也應(yīng)于2018年1月1日符合《規(guī)范》要求。相信在未來(lái)兩年時(shí)間里,,風(fēng)波將席卷整個(gè)醫(yī)械圈,,而不符合規(guī)范者將被淘汰出局。 你,,做好準(zhǔn)備了嗎,?
經(jīng)過(guò)梳理,中國(guó)醫(yī)療器械發(fā)現(xiàn),,此次督查不可不謂時(shí)間緊,、任務(wù)重,、動(dòng)真格。 比如安徽省要求在今年6月底前就完成所有第三類(lèi)醫(yī)療器械生產(chǎn)企業(yè)質(zhì)量管理體系的全面檢查,。而浙江全省236家第三類(lèi)醫(yī)療器械生產(chǎn)企業(yè)中,,已有20家被限期整改,6家被停產(chǎn)整改,,還有4家主動(dòng)停產(chǎn),,1家注銷(xiāo)等等,占比近15%,。預(yù)測(cè)日后會(huì)有更多省份陸續(xù)展開(kāi)相關(guān)督查工作,,新一輪督查風(fēng)暴即將來(lái)襲! 此外,,國(guó)家局要求,,第三類(lèi)以外的其他醫(yī)療器械生產(chǎn)企業(yè)也應(yīng)于2018年1月1日符合《規(guī)范》要求。相信在未來(lái)兩年時(shí)間里,,風(fēng)波將席卷整個(gè)醫(yī)械圈,,而不符合規(guī)范者將被淘汰出局。 你,,做好準(zhǔn)備了嗎,?
 備注:未經(jīng)特殊說(shuō)明的均為共有關(guān)鍵項(xiàng)目,,各類(lèi)型企業(yè)均需遵守的,,以下同。 2,、廠(chǎng)房與設(shè)施,,計(jì)8項(xiàng)
備注:未經(jīng)特殊說(shuō)明的均為共有關(guān)鍵項(xiàng)目,,各類(lèi)型企業(yè)均需遵守的,,以下同。 2,、廠(chǎng)房與設(shè)施,,計(jì)8項(xiàng) 
 3、設(shè)備,,計(jì)3項(xiàng)
3、設(shè)備,,計(jì)3項(xiàng)  4,、文件管理,計(jì)2項(xiàng)
4,、文件管理,計(jì)2項(xiàng)  5,、設(shè)計(jì)開(kāi)發(fā),,計(jì)2項(xiàng)
5,、設(shè)計(jì)開(kāi)發(fā),,計(jì)2項(xiàng)  6、采購(gòu),,計(jì)12項(xiàng)
6、采購(gòu),,計(jì)12項(xiàng) 

 7,、生產(chǎn)管理,計(jì)11項(xiàng)
7,、生產(chǎn)管理,計(jì)11項(xiàng) 
 8,、質(zhì)量控制,,計(jì)8項(xiàng)
8,、質(zhì)量控制,,計(jì)8項(xiàng) 
 9、銷(xiāo)售和售后服務(wù),,計(jì)1項(xiàng) *9.1.1 應(yīng)當(dāng)建立產(chǎn)品銷(xiāo)售記錄,,并滿(mǎn)足可追溯要求。 10,、不合格品控制,,計(jì)1項(xiàng)
9、銷(xiāo)售和售后服務(wù),,計(jì)1項(xiàng) *9.1.1 應(yīng)當(dāng)建立產(chǎn)品銷(xiāo)售記錄,,并滿(mǎn)足可追溯要求。 10,、不合格品控制,,計(jì)1項(xiàng)  11、不良事件監(jiān)測(cè),、分析和改進(jìn),,計(jì)4項(xiàng)
11、不良事件監(jiān)測(cè),、分析和改進(jìn),,計(jì)4項(xiàng)  經(jīng)過(guò)梳理,中國(guó)醫(yī)療器械發(fā)現(xiàn),,此次督查不可不謂時(shí)間緊,、任務(wù)重,、動(dòng)真格。 比如安徽省要求在今年6月底前就完成所有第三類(lèi)醫(yī)療器械生產(chǎn)企業(yè)質(zhì)量管理體系的全面檢查,。而浙江全省236家第三類(lèi)醫(yī)療器械生產(chǎn)企業(yè)中,,已有20家被限期整改,6家被停產(chǎn)整改,,還有4家主動(dòng)停產(chǎn),,1家注銷(xiāo)等等,占比近15%,。預(yù)測(cè)日后會(huì)有更多省份陸續(xù)展開(kāi)相關(guān)督查工作,,新一輪督查風(fēng)暴即將來(lái)襲! 此外,,國(guó)家局要求,,第三類(lèi)以外的其他醫(yī)療器械生產(chǎn)企業(yè)也應(yīng)于2018年1月1日符合《規(guī)范》要求。相信在未來(lái)兩年時(shí)間里,,風(fēng)波將席卷整個(gè)醫(yī)械圈,,而不符合規(guī)范者將被淘汰出局。 你,,做好準(zhǔn)備了嗎,?
經(jīng)過(guò)梳理,中國(guó)醫(yī)療器械發(fā)現(xiàn),,此次督查不可不謂時(shí)間緊,、任務(wù)重,、動(dòng)真格。 比如安徽省要求在今年6月底前就完成所有第三類(lèi)醫(yī)療器械生產(chǎn)企業(yè)質(zhì)量管理體系的全面檢查,。而浙江全省236家第三類(lèi)醫(yī)療器械生產(chǎn)企業(yè)中,,已有20家被限期整改,6家被停產(chǎn)整改,,還有4家主動(dòng)停產(chǎn),,1家注銷(xiāo)等等,占比近15%,。預(yù)測(cè)日后會(huì)有更多省份陸續(xù)展開(kāi)相關(guān)督查工作,,新一輪督查風(fēng)暴即將來(lái)襲! 此外,,國(guó)家局要求,,第三類(lèi)以外的其他醫(yī)療器械生產(chǎn)企業(yè)也應(yīng)于2018年1月1日符合《規(guī)范》要求。相信在未來(lái)兩年時(shí)間里,,風(fēng)波將席卷整個(gè)醫(yī)械圈,,而不符合規(guī)范者將被淘汰出局。 你,,做好準(zhǔn)備了嗎,?






