2018年藥物政策領(lǐng)域遺留下來最大的懸念,,莫過于國(guó)家輔助用藥目錄的遴選工作,。2018年12月12日,國(guó)家衛(wèi)健委發(fā)布《關(guān)于做好輔助用藥臨床應(yīng)用管理有關(guān)工作的通知》,,宣布制定國(guó)家版輔助用藥目錄,。
據(jù)不完全統(tǒng)計(jì),截至目前,,安徽,、海南、新疆,、河北,、上海、廣西等省市已經(jīng)陸續(xù)下發(fā)通知,,要求本省市醫(yī)療機(jī)構(gòu)提交輔助用藥品種清單,?!皣?guó)輔目錄”出臺(tái)已迫在眉睫。
值得注意的是,,“輔助用藥”一直沒有明確界定篩選標(biāo)準(zhǔn)及范圍,。此前,業(yè)界一度認(rèn)為最終的目錄會(huì)根據(jù)按照藥品銷售額進(jìn)行遴選,,并在目錄執(zhí)行后受到更嚴(yán)格限制,。丹紅注射液等高銷量的中藥輔助用藥大品種將面臨巨大沖擊。
在1月19日,,由E藥經(jīng)理人,、中國(guó)醫(yī)療健康產(chǎn)業(yè)投資50人論壇聯(lián)合主辦的“2019中國(guó)醫(yī)藥產(chǎn)業(yè)新年展望會(huì)”上,國(guó)家衛(wèi)健委衛(wèi)生發(fā)展研究中心衛(wèi)生技術(shù)評(píng)估室副研究員劉躍華明確回應(yīng)了業(yè)界對(duì)于國(guó)家輔助用藥篩選標(biāo)準(zhǔn)的困惑,。
劉躍華表示,,國(guó)家輔助用藥目錄的遴選方式會(huì)注重臨床實(shí)際價(jià)值。根據(jù)藥品臨床評(píng)價(jià)結(jié)果,,出臺(tái)“正面清單”和“負(fù)面清單”,。正面的清單是鼓勵(lì)優(yōu)先采購的清單,正面清單內(nèi)的輔助用藥是有效且正面的,,是應(yīng)該購買和使用的,,或者是處理某一種疾病不良反應(yīng)不可或缺的藥品,又或者是兒童的,、特殊疾病需要的藥品,。同時(shí)也需要一個(gè)負(fù)面清單。如果企業(yè)本身的藥品通過循證證據(jù)證明沒有任何效果,,或者沒有證明它比別的藥有更好的效果,,那么它是價(jià)值比較低的,、不優(yōu)先采購的負(fù)面的清單,,這樣才能保證我們?cè)谂R床上控制輔助用藥的合理需求。
而輔助用藥“正面清單”和“負(fù)面清單”的標(biāo)準(zhǔn)如何區(qū)分,?2019年1月17日,,中華藥學(xué)會(huì)正式發(fā)布了中藥大品種科技競(jìng)爭(zhēng)力報(bào)告(2018版),該報(bào)告全景式展示了中藥大品種科技競(jìng)爭(zhēng)力概況,。該報(bào)告包含全品類百強(qiáng)榜,、非注射百強(qiáng)榜、各省區(qū)排行榜第一名,、各治療領(lǐng)域前三名等榜單,,而榜單中有不少中藥輔助用藥特別是中藥注射劑品種上榜。
所謂科技競(jìng)爭(zhēng)力,,集中體現(xiàn)在中成藥產(chǎn)品的臨床價(jià)值和科學(xué)價(jià)值,,是中成藥產(chǎn)業(yè)和臨床價(jià)值的一個(gè)綜合考量,。而國(guó)家輔助用藥目錄的遴選方式同樣注重臨床實(shí)際價(jià)值,會(huì)根據(jù)藥品臨床評(píng)價(jià)結(jié)果,,形成“正面清單”和“負(fù)面清單”,。
借由科技競(jìng)爭(zhēng)力榜單,可以評(píng)估目前中成藥產(chǎn)品的市場(chǎng)價(jià)值,、臨床價(jià)值和科學(xué)價(jià)值綜合水平的高低,,借此榜單能摸索出國(guó)家輔助用藥目錄遴選可能的演繹邏輯。
1,、5維度評(píng)估中藥注射劑
整個(gè)科技競(jìng)爭(zhēng)力榜單以“臨床價(jià)值大,、科學(xué)價(jià)值強(qiáng)、市場(chǎng)價(jià)值高”三個(gè)維度,,遴選2018 年科技競(jìng)爭(zhēng)力評(píng)價(jià)的中藥大品種,。該榜單設(shè)置了5個(gè)一類指標(biāo),涉及“科技投入”“科技產(chǎn)出”“科技獎(jiǎng)勵(lì)”“其他單項(xiàng)”以及“核減指標(biāo)”5個(gè)方面,。其中,,“核減指標(biāo)”無疑是媒體和公眾最常關(guān)注到一個(gè)指標(biāo),涉及到國(guó)家藥監(jiān)部門發(fā)布的不良事件通報(bào),、強(qiáng)制修訂說明書,、質(zhì)量通告等負(fù)面通報(bào)。而該指標(biāo)僅為5個(gè)評(píng)估方面中的一部分,,無疑能夠平衡公共安全和科技性上的考量,。
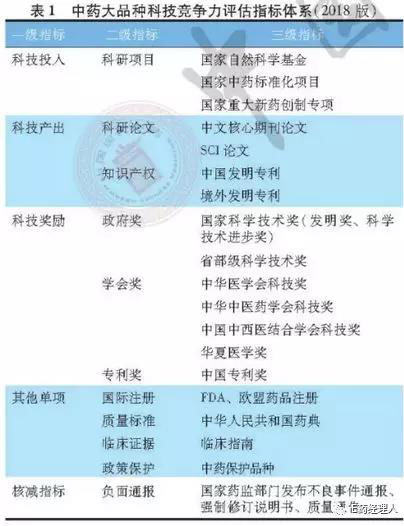
最終確定入圍 2018 年中藥大品種科技競(jìng)爭(zhēng)力評(píng)價(jià)的 569 個(gè)產(chǎn)品,涉及 376 家企業(yè),、 520 個(gè)品種,。
中藥大品種(全品類)科技競(jìng)爭(zhēng)力百強(qiáng)榜涉及的中藥注射劑
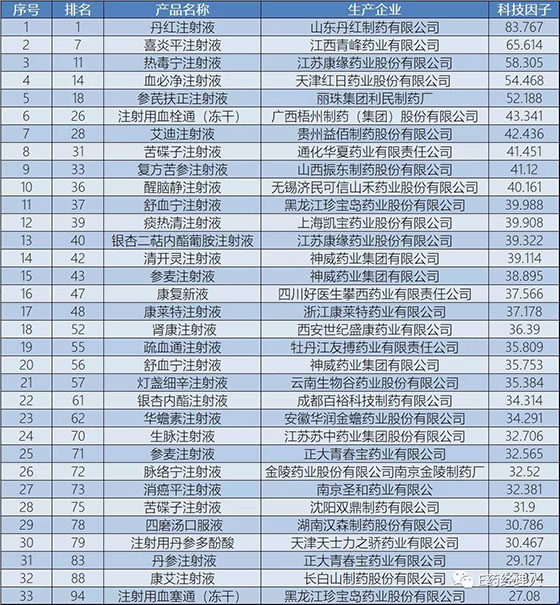
在中藥大品種科技競(jìng)爭(zhēng)力報(bào)告(2018版)核心榜單中藥大品種百強(qiáng)榜中,此前屢受質(zhì)疑的輔助用藥中藥注射劑頻頻露面,,占據(jù)了100強(qiáng)中33席,。
步長(zhǎng)制藥主力產(chǎn)品丹紅注射劑躲得科技競(jìng)爭(zhēng)力百強(qiáng)榜冠軍,由此可知,,丹紅注射劑在臨床價(jià)值,、科學(xué)價(jià)值及市場(chǎng)價(jià)值3方面相較其他中成藥有過人之處。但丹紅注射液此前已相繼被多個(gè)省份地區(qū)納入輔助與重點(diǎn)監(jiān)控用藥目錄,。并且,,丹紅注射液更是被限二級(jí)及以上醫(yī)療機(jī)構(gòu)并有明確的缺血性心腦血管疾病急性發(fā)作證據(jù)的重癥患者使用。
在政策收緊壓力之下,,丹紅注射劑的業(yè)績(jī)表現(xiàn)也在明顯下滑,。年報(bào)顯示,2017年步長(zhǎng)制藥生產(chǎn)的兩種丹紅注射液劑型(分別為10ml/支、20ml/支)生產(chǎn)量分別同比下降11.35%,、11.33%,,銷售量下降幅度分別為1.66%、1.35%,。
排名第六的喜炎平注射液此前的銷售也遭遇了很大的波折,。喜炎平注射液是江西青峰藥業(yè)的獨(dú)家品種,廣泛用于成人各類感染性疾病以及兒童呼吸系統(tǒng)感染,、手足口病,、感染性腹瀉等領(lǐng)域,,是原衛(wèi)生部《手足口病診療指南》、《甲型H1N1流感診療方案》及《發(fā)熱伴血小板減少綜合癥防治指南》的推薦用藥,。
2016年,,喜炎平注射液在清熱解毒類中藥注射液銷售領(lǐng)域排名前三,。相關(guān)資料顯示,2015年青峰藥業(yè)來自喜炎平注射液收入為35億元,;2016年,喜炎平注射液年銷量約為2億支,。2017年,喜炎平注射液被國(guó)家食藥監(jiān)總局勒令停產(chǎn)待檢兩個(gè)多月,,后在2017年11月30日經(jīng)江西省食藥監(jiān)同意恢復(fù)生產(chǎn),。但在恢復(fù)生產(chǎn)之后,,喜炎平注射液仍然出現(xiàn)了不少的不良事件。
除丹紅注射液,、喜炎平注射液兩個(gè)品種之外,熱毒寧注射液,、血必凈注射液,、參芪扶正注射液等中藥注射劑品種都遭遇了醫(yī)保報(bào)銷限制、醫(yī)療機(jī)構(gòu)使用范圍限制、修改藥品使用說明書等一系列限制,,銷量也在近段時(shí)間出現(xiàn)了明顯下滑。
PDB數(shù)據(jù)顯示,,2017年銷售金額前20位藥品中,中藥注射劑占比超過36%,。瑞銀估算中藥注射劑+輔助用藥整體終端金額約1000億,,占比5%-10%。而在醫(yī)??刭M(fèi)并納入更多創(chuàng)新藥的政策大環(huán)境下,需要清退出更多“神藥”為療效確切的藥品騰挪出資金空間,。
雖然中藥注射劑作為輔助用藥一種因?yàn)轭l繁出現(xiàn)藥品安全事件而在過去一段時(shí)間內(nèi)受到了越來越緊的政策限制,但科技競(jìng)爭(zhēng)力榜單并未“厚此薄彼”,,而同時(shí)考量“科技投入”、“科技產(chǎn)出”,、“科技獎(jiǎng)勵(lì)”、“國(guó)際注冊(cè)”,、“質(zhì)量標(biāo)準(zhǔn)”、“臨床證據(jù)”,、“政策保護(hù)”等多個(gè)方面,進(jìn)行了比較全面的評(píng)估,。
即將出臺(tái)的國(guó)家輔助用藥目錄也并非一味禁止輔助用藥的臨床使用,而是形成“負(fù)面清單”和“正面清單”,,“正面清單”內(nèi)的輔助用藥鼓勵(lì)優(yōu)先采購,“負(fù)面清單”內(nèi)的輔助藥限制采購,。中藥大品種科技競(jìng)爭(zhēng)力榜提供了對(duì)于中藥注射劑相對(duì)多維度的評(píng)估,能夠作為國(guó)家輔助用藥目錄出臺(tái)前的一個(gè)參考標(biāo)準(zhǔn),。







