已經(jīng)結(jié)束的 2015 是藥品政策劇變、行業(yè)震蕩的一年,,震蕩之余,,我們依然要保持著向上的狀態(tài),用大數(shù)據(jù)來闡述這一年 CDE 的真實(shí)審評情況,。 根據(jù) Insight-China Pharma Data 數(shù)據(jù)庫統(tǒng)計,,2015 年 CDE 共承辦新的藥品注冊受理 8217 個(以受理號計,見圖 1),。 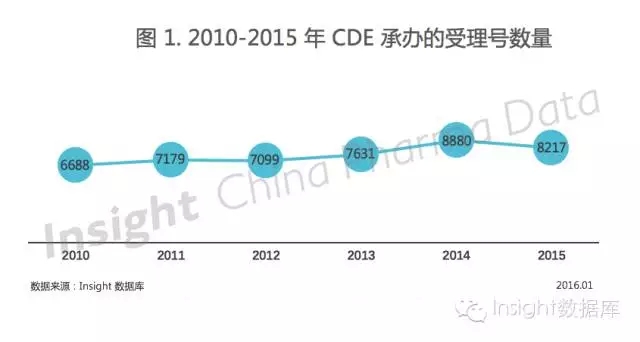 如圖 1所示,,2014 年申報受理數(shù)量達(dá)到最高峰,2015 年則有所下降,。據(jù) Insight 統(tǒng)計,,2015 年上半年申報受理數(shù)量還略高于 2014 年同期水平,下半年就下降了,,可見 2015 年解決藥品積壓受理的種種政策起到了一定作用,。 就 2015 年而言,1-7 月,,除了 5 月受注冊漲價影響稍有減少以外,,CDE 承辦的受理號數(shù)量一直總體持續(xù)增長,8 月出臺一系列的解決積壓受理政策和意見之后,,申報數(shù)量整體下降明顯,。
如圖 1所示,,2014 年申報受理數(shù)量達(dá)到最高峰,2015 年則有所下降,。據(jù) Insight 統(tǒng)計,,2015 年上半年申報受理數(shù)量還略高于 2014 年同期水平,下半年就下降了,,可見 2015 年解決藥品積壓受理的種種政策起到了一定作用,。 就 2015 年而言,1-7 月,,除了 5 月受注冊漲價影響稍有減少以外,,CDE 承辦的受理號數(shù)量一直總體持續(xù)增長,8 月出臺一系列的解決積壓受理政策和意見之后,,申報數(shù)量整體下降明顯,。  如圖 2 所示,各個申請類型中,,新藥和仿制藥的申報數(shù)量受政策影響波動較大,,而進(jìn)口藥品的申報數(shù)量則相對平穩(wěn)一些。 受到 7-12 月自查核查風(fēng)暴和 12 月仿制藥生物等效性試驗(yàn)備案管理備案政策實(shí)施的影響,,12 月新藥和仿制藥申報數(shù)量都有所下降,,補(bǔ)充申請和進(jìn)口申請則顯著增加??磥韲鴥?nèi)企業(yè)日子不好過,,而外資企業(yè)不太受影響。 以下,,分別來回顧 2015 年化藥,、中藥、生物制品的申報受理情況,。 一,、化藥申報受理情況 仿制藥,、進(jìn)口藥申報分別縮水 10.5% 和 18.4% 前面已經(jīng)提過,2015 年的整體申報數(shù)量相比 2014 年是有所下降的,,其中化藥占了大部分,。 具體看來,對比化藥新藥,、仿制藥和進(jìn)口藥的申報數(shù)量,,仿制藥和進(jìn)口藥申報分別有 10.5% 和 18.4% 的縮水;新藥申報仍然上漲,,但可以看出增速有所放緩,。
如圖 2 所示,各個申請類型中,,新藥和仿制藥的申報數(shù)量受政策影響波動較大,,而進(jìn)口藥品的申報數(shù)量則相對平穩(wěn)一些。 受到 7-12 月自查核查風(fēng)暴和 12 月仿制藥生物等效性試驗(yàn)備案管理備案政策實(shí)施的影響,,12 月新藥和仿制藥申報數(shù)量都有所下降,,補(bǔ)充申請和進(jìn)口申請則顯著增加??磥韲鴥?nèi)企業(yè)日子不好過,,而外資企業(yè)不太受影響。 以下,,分別來回顧 2015 年化藥,、中藥、生物制品的申報受理情況,。 一,、化藥申報受理情況 仿制藥,、進(jìn)口藥申報分別縮水 10.5% 和 18.4% 前面已經(jīng)提過,2015 年的整體申報數(shù)量相比 2014 年是有所下降的,,其中化藥占了大部分,。 具體看來,對比化藥新藥,、仿制藥和進(jìn)口藥的申報數(shù)量,,仿制藥和進(jìn)口藥申報分別有 10.5% 和 18.4% 的縮水;新藥申報仍然上漲,,但可以看出增速有所放緩,。 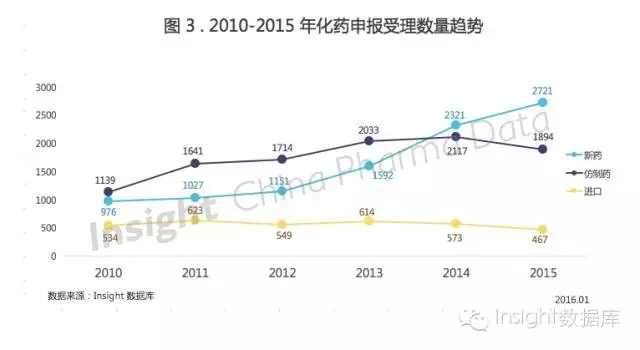 1、新藥申報受理情況 2015 年 1-12 月,,平均每月有 16 個 1.1 類新藥注冊申請被 CDE 受理,,且總體看來每月的申報數(shù)量比較平穩(wěn)(見圖 4)。 3.1 類新藥申報數(shù)量波動很大,,7 月達(dá)最高峰,,8 月之后 3.1 類新藥申報數(shù)量趨勢明顯走低,12 月降至最低,,相差達(dá) 2.5 倍,。
1、新藥申報受理情況 2015 年 1-12 月,,平均每月有 16 個 1.1 類新藥注冊申請被 CDE 受理,,且總體看來每月的申報數(shù)量比較平穩(wěn)(見圖 4)。 3.1 類新藥申報數(shù)量波動很大,,7 月達(dá)最高峰,,8 月之后 3.1 類新藥申報數(shù)量趨勢明顯走低,12 月降至最低,,相差達(dá) 2.5 倍,。  2015 年 3.1 類新藥的申報熱情暫時被化藥注冊新分類和仿制藥一致性評價澆滅了不少,但瞄準(zhǔn) 3.1 類新藥的企業(yè)會坐以待斃還是一如既往熱衷這類候選藥物,,目前還不能下定論,。 1)1.1 類新藥申報持續(xù)增長 根據(jù) Insight 數(shù)據(jù)庫統(tǒng)計,新申報的化藥 1.1 類新藥申請以受理號計有 201 個,,數(shù)量在持續(xù)增長,。 2015 年新申報的 1.1 類新藥共涉及 76 個品種,其中僅江蘇恒瑞的磷酸瑞格列汀片和北京康辰藥業(yè)的注射用鹽酸諾拉曲塞申報上市,,目前瑞格列汀已完成了藥理毒理專業(yè)項審評,排在 NDA 隊列的 274 位,;而諾拉曲塞的審評結(jié)論則為批準(zhǔn)臨床,。 每個月新申報的 1.1 類都在 Insight 每月審評報告中有詳細(xì)介紹,在此不贅述,。 2)3.1 類首家搶仿的熱潮與冷卻 3.1 類新藥除了申報總數(shù)受到政策變化影響以外,,首家搶仿申報也經(jīng)歷了一輪熱潮與冷卻。 如圖 5 所示,,8 月之前,,平均每月有 3-4 個品種被國內(nèi)企業(yè)首家搶仿,其中不乏原研企業(yè)在全球剛批準(zhǔn)上市,,國內(nèi)企業(yè)就已申報搶仿的品種,。 8 月之后,,搶仿數(shù)量明顯下降,12 月雖有 3.1 類品種申報,,但首家搶仿卻是空白,。
2015 年 3.1 類新藥的申報熱情暫時被化藥注冊新分類和仿制藥一致性評價澆滅了不少,但瞄準(zhǔn) 3.1 類新藥的企業(yè)會坐以待斃還是一如既往熱衷這類候選藥物,,目前還不能下定論,。 1)1.1 類新藥申報持續(xù)增長 根據(jù) Insight 數(shù)據(jù)庫統(tǒng)計,新申報的化藥 1.1 類新藥申請以受理號計有 201 個,,數(shù)量在持續(xù)增長,。 2015 年新申報的 1.1 類新藥共涉及 76 個品種,其中僅江蘇恒瑞的磷酸瑞格列汀片和北京康辰藥業(yè)的注射用鹽酸諾拉曲塞申報上市,,目前瑞格列汀已完成了藥理毒理專業(yè)項審評,排在 NDA 隊列的 274 位,;而諾拉曲塞的審評結(jié)論則為批準(zhǔn)臨床,。 每個月新申報的 1.1 類都在 Insight 每月審評報告中有詳細(xì)介紹,在此不贅述,。 2)3.1 類首家搶仿的熱潮與冷卻 3.1 類新藥除了申報總數(shù)受到政策變化影響以外,,首家搶仿申報也經(jīng)歷了一輪熱潮與冷卻。 如圖 5 所示,,8 月之前,,平均每月有 3-4 個品種被國內(nèi)企業(yè)首家搶仿,其中不乏原研企業(yè)在全球剛批準(zhǔn)上市,,國內(nèi)企業(yè)就已申報搶仿的品種,。 8 月之后,,搶仿數(shù)量明顯下降,12 月雖有 3.1 類品種申報,,但首家搶仿卻是空白,。 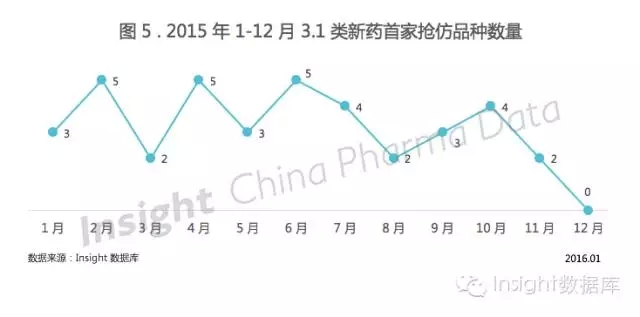 2、仿制藥申報受理情況 仿制藥申報數(shù)量降幅為 10.5% 2015 年 11 月 18 日,,CFDA 發(fā)布征求《關(guān)于開展仿制藥質(zhì)量和療效一致性評價的意見(征求意見稿)》意見,。 這意味著仿制藥質(zhì)量終于得到重視,隨之而來的是企業(yè)研發(fā)成本的增加,,仿制藥將不再那么容易被?仿制?,,加上規(guī)定期限內(nèi)未完成一致性評價注銷文號或動作慢了就無法在集中采購中勝出的種種限制,2015 年仿制藥申報數(shù)量的減少在意料之中,。 事實(shí)上,,從 2014 年開始,仿制藥申報量已經(jīng)減少,,至 2015 年降幅達(dá) 10.5%,。 3、進(jìn)口藥申報受理情況 年末進(jìn)口藥申報數(shù)量開始爬升 今年的政策局面無疑是利好外資企業(yè)的,,無論是提高仿制藥質(zhì)量使得國內(nèi)企業(yè)要面臨許多挑戰(zhàn),,還是臨床試驗(yàn)自查核查的撤回風(fēng)暴,外資企業(yè)都損失較小,。 雖然 2015 年進(jìn)口藥申報量不如 2014 年,,但從 2015 年 1-12 月的進(jìn)口藥申報趨勢來看(如圖 2),12 月進(jìn)口藥申報量已經(jīng)開始上升,,且 12 月首次申報進(jìn)口的數(shù)據(jù)大多為全球在研藥物,。 可見,在這樣利好的局面下,,外資企業(yè)已經(jīng)開始發(fā)力,,來鞏固在華的業(yè)務(wù)。 二,、中藥申報受理情況 中藥申報數(shù)量明顯下降 根據(jù) Insight 數(shù)據(jù)庫,,2015 年申報的中藥申請以受理號計共 377 個,相比 2014 年的 531 個申請,,申報明顯下降,。 2015 年的具體申請類型如圖 6 所示:
2、仿制藥申報受理情況 仿制藥申報數(shù)量降幅為 10.5% 2015 年 11 月 18 日,,CFDA 發(fā)布征求《關(guān)于開展仿制藥質(zhì)量和療效一致性評價的意見(征求意見稿)》意見,。 這意味著仿制藥質(zhì)量終于得到重視,隨之而來的是企業(yè)研發(fā)成本的增加,,仿制藥將不再那么容易被?仿制?,,加上規(guī)定期限內(nèi)未完成一致性評價注銷文號或動作慢了就無法在集中采購中勝出的種種限制,2015 年仿制藥申報數(shù)量的減少在意料之中,。 事實(shí)上,,從 2014 年開始,仿制藥申報量已經(jīng)減少,,至 2015 年降幅達(dá) 10.5%,。 3、進(jìn)口藥申報受理情況 年末進(jìn)口藥申報數(shù)量開始爬升 今年的政策局面無疑是利好外資企業(yè)的,,無論是提高仿制藥質(zhì)量使得國內(nèi)企業(yè)要面臨許多挑戰(zhàn),,還是臨床試驗(yàn)自查核查的撤回風(fēng)暴,外資企業(yè)都損失較小,。 雖然 2015 年進(jìn)口藥申報量不如 2014 年,,但從 2015 年 1-12 月的進(jìn)口藥申報趨勢來看(如圖 2),12 月進(jìn)口藥申報量已經(jīng)開始上升,,且 12 月首次申報進(jìn)口的數(shù)據(jù)大多為全球在研藥物,。 可見,在這樣利好的局面下,,外資企業(yè)已經(jīng)開始發(fā)力,,來鞏固在華的業(yè)務(wù)。 二,、中藥申報受理情況 中藥申報數(shù)量明顯下降 根據(jù) Insight 數(shù)據(jù)庫,,2015 年申報的中藥申請以受理號計共 377 個,相比 2014 年的 531 個申請,,申報明顯下降,。 2015 年的具體申請類型如圖 6 所示: 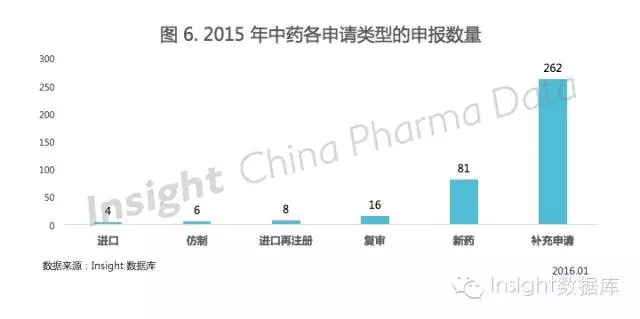 三、生物制品申報受理情況 生物制品市場擴(kuò)容 18.6% 2015 年申報的生物制品申請以受理號計共有 558 個,,相比 2014 年的 454 個申請,,申報量漲了 18.6%。 2015 年的具體申請類型如圖 7 所示:
三、生物制品申報受理情況 生物制品市場擴(kuò)容 18.6% 2015 年申報的生物制品申請以受理號計共有 558 個,,相比 2014 年的 454 個申請,,申報量漲了 18.6%。 2015 年的具體申請類型如圖 7 所示: 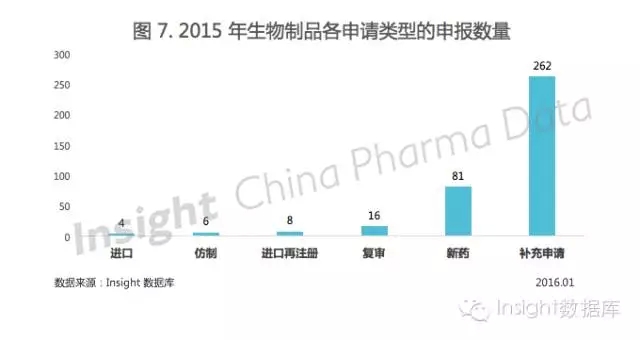 其中,,1 類生物制品以受理號計共 37 個,。 1 類生物制品的 35 個臨床申請中,,有 3 個品種在一年內(nèi)獲得了臨床批件,分別是北京科興的 Sabin 株脊髓灰質(zhì)炎滅活疫苗(Vero 細(xì)胞),、泰州君實(shí)的重組人源化抗 PD-1 單克隆抗體,、以及軍科院生物工程研究所研發(fā)的重組埃博拉病毒病疫苗。 另外,,今年只有 2 個 1 類生物制品申報上市,,分別為上海仁會生物的貝那魯肽注射液、成都康弘生物的康柏西普眼用注射液,。 上海仁會生物的貝那魯肽是重組人胰高血糖素類多肽-1,,該藥上市申報受理號在 722 公告列表中,目前還沒有結(jié)論,。 康柏西普是 2013 年批準(zhǔn)用于治療濕性年齡相關(guān)性黃斑變性的新藥,,2015 年新的上市申請有可能為新適應(yīng)癥。 至此,,2015 年中國藥品申報已經(jīng)盤點(diǎn)完,。
其中,,1 類生物制品以受理號計共 37 個,。 1 類生物制品的 35 個臨床申請中,,有 3 個品種在一年內(nèi)獲得了臨床批件,分別是北京科興的 Sabin 株脊髓灰質(zhì)炎滅活疫苗(Vero 細(xì)胞),、泰州君實(shí)的重組人源化抗 PD-1 單克隆抗體,、以及軍科院生物工程研究所研發(fā)的重組埃博拉病毒病疫苗。 另外,,今年只有 2 個 1 類生物制品申報上市,,分別為上海仁會生物的貝那魯肽注射液、成都康弘生物的康柏西普眼用注射液,。 上海仁會生物的貝那魯肽是重組人胰高血糖素類多肽-1,,該藥上市申報受理號在 722 公告列表中,目前還沒有結(jié)論,。 康柏西普是 2013 年批準(zhǔn)用于治療濕性年齡相關(guān)性黃斑變性的新藥,,2015 年新的上市申請有可能為新適應(yīng)癥。 至此,,2015 年中國藥品申報已經(jīng)盤點(diǎn)完,。
 如圖 1所示,,2014 年申報受理數(shù)量達(dá)到最高峰,2015 年則有所下降,。據(jù) Insight 統(tǒng)計,,2015 年上半年申報受理數(shù)量還略高于 2014 年同期水平,下半年就下降了,,可見 2015 年解決藥品積壓受理的種種政策起到了一定作用,。 就 2015 年而言,1-7 月,,除了 5 月受注冊漲價影響稍有減少以外,,CDE 承辦的受理號數(shù)量一直總體持續(xù)增長,8 月出臺一系列的解決積壓受理政策和意見之后,,申報數(shù)量整體下降明顯,。
如圖 1所示,,2014 年申報受理數(shù)量達(dá)到最高峰,2015 年則有所下降,。據(jù) Insight 統(tǒng)計,,2015 年上半年申報受理數(shù)量還略高于 2014 年同期水平,下半年就下降了,,可見 2015 年解決藥品積壓受理的種種政策起到了一定作用,。 就 2015 年而言,1-7 月,,除了 5 月受注冊漲價影響稍有減少以外,,CDE 承辦的受理號數(shù)量一直總體持續(xù)增長,8 月出臺一系列的解決積壓受理政策和意見之后,,申報數(shù)量整體下降明顯,。  如圖 2 所示,各個申請類型中,,新藥和仿制藥的申報數(shù)量受政策影響波動較大,,而進(jìn)口藥品的申報數(shù)量則相對平穩(wěn)一些。 受到 7-12 月自查核查風(fēng)暴和 12 月仿制藥生物等效性試驗(yàn)備案管理備案政策實(shí)施的影響,,12 月新藥和仿制藥申報數(shù)量都有所下降,,補(bǔ)充申請和進(jìn)口申請則顯著增加??磥韲鴥?nèi)企業(yè)日子不好過,,而外資企業(yè)不太受影響。 以下,,分別來回顧 2015 年化藥,、中藥、生物制品的申報受理情況,。 一,、化藥申報受理情況 仿制藥,、進(jìn)口藥申報分別縮水 10.5% 和 18.4% 前面已經(jīng)提過,2015 年的整體申報數(shù)量相比 2014 年是有所下降的,,其中化藥占了大部分,。 具體看來,對比化藥新藥,、仿制藥和進(jìn)口藥的申報數(shù)量,,仿制藥和進(jìn)口藥申報分別有 10.5% 和 18.4% 的縮水;新藥申報仍然上漲,,但可以看出增速有所放緩,。
如圖 2 所示,各個申請類型中,,新藥和仿制藥的申報數(shù)量受政策影響波動較大,,而進(jìn)口藥品的申報數(shù)量則相對平穩(wěn)一些。 受到 7-12 月自查核查風(fēng)暴和 12 月仿制藥生物等效性試驗(yàn)備案管理備案政策實(shí)施的影響,,12 月新藥和仿制藥申報數(shù)量都有所下降,,補(bǔ)充申請和進(jìn)口申請則顯著增加??磥韲鴥?nèi)企業(yè)日子不好過,,而外資企業(yè)不太受影響。 以下,,分別來回顧 2015 年化藥,、中藥、生物制品的申報受理情況,。 一,、化藥申報受理情況 仿制藥,、進(jìn)口藥申報分別縮水 10.5% 和 18.4% 前面已經(jīng)提過,2015 年的整體申報數(shù)量相比 2014 年是有所下降的,,其中化藥占了大部分,。 具體看來,對比化藥新藥,、仿制藥和進(jìn)口藥的申報數(shù)量,,仿制藥和進(jìn)口藥申報分別有 10.5% 和 18.4% 的縮水;新藥申報仍然上漲,,但可以看出增速有所放緩,。  1、新藥申報受理情況 2015 年 1-12 月,,平均每月有 16 個 1.1 類新藥注冊申請被 CDE 受理,,且總體看來每月的申報數(shù)量比較平穩(wěn)(見圖 4)。 3.1 類新藥申報數(shù)量波動很大,,7 月達(dá)最高峰,,8 月之后 3.1 類新藥申報數(shù)量趨勢明顯走低,12 月降至最低,,相差達(dá) 2.5 倍,。
1、新藥申報受理情況 2015 年 1-12 月,,平均每月有 16 個 1.1 類新藥注冊申請被 CDE 受理,,且總體看來每月的申報數(shù)量比較平穩(wěn)(見圖 4)。 3.1 類新藥申報數(shù)量波動很大,,7 月達(dá)最高峰,,8 月之后 3.1 類新藥申報數(shù)量趨勢明顯走低,12 月降至最低,,相差達(dá) 2.5 倍,。  2015 年 3.1 類新藥的申報熱情暫時被化藥注冊新分類和仿制藥一致性評價澆滅了不少,但瞄準(zhǔn) 3.1 類新藥的企業(yè)會坐以待斃還是一如既往熱衷這類候選藥物,,目前還不能下定論,。 1)1.1 類新藥申報持續(xù)增長 根據(jù) Insight 數(shù)據(jù)庫統(tǒng)計,新申報的化藥 1.1 類新藥申請以受理號計有 201 個,,數(shù)量在持續(xù)增長,。 2015 年新申報的 1.1 類新藥共涉及 76 個品種,其中僅江蘇恒瑞的磷酸瑞格列汀片和北京康辰藥業(yè)的注射用鹽酸諾拉曲塞申報上市,,目前瑞格列汀已完成了藥理毒理專業(yè)項審評,排在 NDA 隊列的 274 位,;而諾拉曲塞的審評結(jié)論則為批準(zhǔn)臨床,。 每個月新申報的 1.1 類都在 Insight 每月審評報告中有詳細(xì)介紹,在此不贅述,。 2)3.1 類首家搶仿的熱潮與冷卻 3.1 類新藥除了申報總數(shù)受到政策變化影響以外,,首家搶仿申報也經(jīng)歷了一輪熱潮與冷卻。 如圖 5 所示,,8 月之前,,平均每月有 3-4 個品種被國內(nèi)企業(yè)首家搶仿,其中不乏原研企業(yè)在全球剛批準(zhǔn)上市,,國內(nèi)企業(yè)就已申報搶仿的品種,。 8 月之后,,搶仿數(shù)量明顯下降,12 月雖有 3.1 類品種申報,,但首家搶仿卻是空白,。
2015 年 3.1 類新藥的申報熱情暫時被化藥注冊新分類和仿制藥一致性評價澆滅了不少,但瞄準(zhǔn) 3.1 類新藥的企業(yè)會坐以待斃還是一如既往熱衷這類候選藥物,,目前還不能下定論,。 1)1.1 類新藥申報持續(xù)增長 根據(jù) Insight 數(shù)據(jù)庫統(tǒng)計,新申報的化藥 1.1 類新藥申請以受理號計有 201 個,,數(shù)量在持續(xù)增長,。 2015 年新申報的 1.1 類新藥共涉及 76 個品種,其中僅江蘇恒瑞的磷酸瑞格列汀片和北京康辰藥業(yè)的注射用鹽酸諾拉曲塞申報上市,,目前瑞格列汀已完成了藥理毒理專業(yè)項審評,排在 NDA 隊列的 274 位,;而諾拉曲塞的審評結(jié)論則為批準(zhǔn)臨床,。 每個月新申報的 1.1 類都在 Insight 每月審評報告中有詳細(xì)介紹,在此不贅述,。 2)3.1 類首家搶仿的熱潮與冷卻 3.1 類新藥除了申報總數(shù)受到政策變化影響以外,,首家搶仿申報也經(jīng)歷了一輪熱潮與冷卻。 如圖 5 所示,,8 月之前,,平均每月有 3-4 個品種被國內(nèi)企業(yè)首家搶仿,其中不乏原研企業(yè)在全球剛批準(zhǔn)上市,,國內(nèi)企業(yè)就已申報搶仿的品種,。 8 月之后,,搶仿數(shù)量明顯下降,12 月雖有 3.1 類品種申報,,但首家搶仿卻是空白,。  2、仿制藥申報受理情況 仿制藥申報數(shù)量降幅為 10.5% 2015 年 11 月 18 日,,CFDA 發(fā)布征求《關(guān)于開展仿制藥質(zhì)量和療效一致性評價的意見(征求意見稿)》意見,。 這意味著仿制藥質(zhì)量終于得到重視,隨之而來的是企業(yè)研發(fā)成本的增加,,仿制藥將不再那么容易被?仿制?,,加上規(guī)定期限內(nèi)未完成一致性評價注銷文號或動作慢了就無法在集中采購中勝出的種種限制,2015 年仿制藥申報數(shù)量的減少在意料之中,。 事實(shí)上,,從 2014 年開始,仿制藥申報量已經(jīng)減少,,至 2015 年降幅達(dá) 10.5%,。 3、進(jìn)口藥申報受理情況 年末進(jìn)口藥申報數(shù)量開始爬升 今年的政策局面無疑是利好外資企業(yè)的,,無論是提高仿制藥質(zhì)量使得國內(nèi)企業(yè)要面臨許多挑戰(zhàn),,還是臨床試驗(yàn)自查核查的撤回風(fēng)暴,外資企業(yè)都損失較小,。 雖然 2015 年進(jìn)口藥申報量不如 2014 年,,但從 2015 年 1-12 月的進(jìn)口藥申報趨勢來看(如圖 2),12 月進(jìn)口藥申報量已經(jīng)開始上升,,且 12 月首次申報進(jìn)口的數(shù)據(jù)大多為全球在研藥物,。 可見,在這樣利好的局面下,,外資企業(yè)已經(jīng)開始發(fā)力,,來鞏固在華的業(yè)務(wù)。 二,、中藥申報受理情況 中藥申報數(shù)量明顯下降 根據(jù) Insight 數(shù)據(jù)庫,,2015 年申報的中藥申請以受理號計共 377 個,相比 2014 年的 531 個申請,,申報明顯下降,。 2015 年的具體申請類型如圖 6 所示:
2、仿制藥申報受理情況 仿制藥申報數(shù)量降幅為 10.5% 2015 年 11 月 18 日,,CFDA 發(fā)布征求《關(guān)于開展仿制藥質(zhì)量和療效一致性評價的意見(征求意見稿)》意見,。 這意味著仿制藥質(zhì)量終于得到重視,隨之而來的是企業(yè)研發(fā)成本的增加,,仿制藥將不再那么容易被?仿制?,,加上規(guī)定期限內(nèi)未完成一致性評價注銷文號或動作慢了就無法在集中采購中勝出的種種限制,2015 年仿制藥申報數(shù)量的減少在意料之中,。 事實(shí)上,,從 2014 年開始,仿制藥申報量已經(jīng)減少,,至 2015 年降幅達(dá) 10.5%,。 3、進(jìn)口藥申報受理情況 年末進(jìn)口藥申報數(shù)量開始爬升 今年的政策局面無疑是利好外資企業(yè)的,,無論是提高仿制藥質(zhì)量使得國內(nèi)企業(yè)要面臨許多挑戰(zhàn),,還是臨床試驗(yàn)自查核查的撤回風(fēng)暴,外資企業(yè)都損失較小,。 雖然 2015 年進(jìn)口藥申報量不如 2014 年,,但從 2015 年 1-12 月的進(jìn)口藥申報趨勢來看(如圖 2),12 月進(jìn)口藥申報量已經(jīng)開始上升,,且 12 月首次申報進(jìn)口的數(shù)據(jù)大多為全球在研藥物,。 可見,在這樣利好的局面下,,外資企業(yè)已經(jīng)開始發(fā)力,,來鞏固在華的業(yè)務(wù)。 二,、中藥申報受理情況 中藥申報數(shù)量明顯下降 根據(jù) Insight 數(shù)據(jù)庫,,2015 年申報的中藥申請以受理號計共 377 個,相比 2014 年的 531 個申請,,申報明顯下降,。 2015 年的具體申請類型如圖 6 所示:  三、生物制品申報受理情況 生物制品市場擴(kuò)容 18.6% 2015 年申報的生物制品申請以受理號計共有 558 個,,相比 2014 年的 454 個申請,,申報量漲了 18.6%。 2015 年的具體申請類型如圖 7 所示:
三、生物制品申報受理情況 生物制品市場擴(kuò)容 18.6% 2015 年申報的生物制品申請以受理號計共有 558 個,,相比 2014 年的 454 個申請,,申報量漲了 18.6%。 2015 年的具體申請類型如圖 7 所示:  其中,,1 類生物制品以受理號計共 37 個,。 1 類生物制品的 35 個臨床申請中,,有 3 個品種在一年內(nèi)獲得了臨床批件,分別是北京科興的 Sabin 株脊髓灰質(zhì)炎滅活疫苗(Vero 細(xì)胞),、泰州君實(shí)的重組人源化抗 PD-1 單克隆抗體,、以及軍科院生物工程研究所研發(fā)的重組埃博拉病毒病疫苗。 另外,,今年只有 2 個 1 類生物制品申報上市,,分別為上海仁會生物的貝那魯肽注射液、成都康弘生物的康柏西普眼用注射液,。 上海仁會生物的貝那魯肽是重組人胰高血糖素類多肽-1,,該藥上市申報受理號在 722 公告列表中,目前還沒有結(jié)論,。 康柏西普是 2013 年批準(zhǔn)用于治療濕性年齡相關(guān)性黃斑變性的新藥,,2015 年新的上市申請有可能為新適應(yīng)癥。 至此,,2015 年中國藥品申報已經(jīng)盤點(diǎn)完,。
其中,,1 類生物制品以受理號計共 37 個,。 1 類生物制品的 35 個臨床申請中,,有 3 個品種在一年內(nèi)獲得了臨床批件,分別是北京科興的 Sabin 株脊髓灰質(zhì)炎滅活疫苗(Vero 細(xì)胞),、泰州君實(shí)的重組人源化抗 PD-1 單克隆抗體,、以及軍科院生物工程研究所研發(fā)的重組埃博拉病毒病疫苗。 另外,,今年只有 2 個 1 類生物制品申報上市,,分別為上海仁會生物的貝那魯肽注射液、成都康弘生物的康柏西普眼用注射液,。 上海仁會生物的貝那魯肽是重組人胰高血糖素類多肽-1,,該藥上市申報受理號在 722 公告列表中,目前還沒有結(jié)論,。 康柏西普是 2013 年批準(zhǔn)用于治療濕性年齡相關(guān)性黃斑變性的新藥,,2015 年新的上市申請有可能為新適應(yīng)癥。 至此,,2015 年中國藥品申報已經(jīng)盤點(diǎn)完,。






