在申報新藥的企業(yè)中,,正大天晴的受理數(shù)最多,為17個,;恒瑞醫(yī)藥和豪森藥業(yè)次之,,分別為12個和8個
▍一批新藥,或提前上市
2月26日,,國家藥審中心擬納入優(yōu)先審評審批欄目下,,增加了7個藥品,共5個品種,,包括北京諾華的達(dá)拉非尼膠囊和曲美替尼片,、信達(dá)生物的阿達(dá)木單抗注射液、萌蒂制藥的普拉曲沙注射液和羅氏的帕妥珠單抗注射液,。
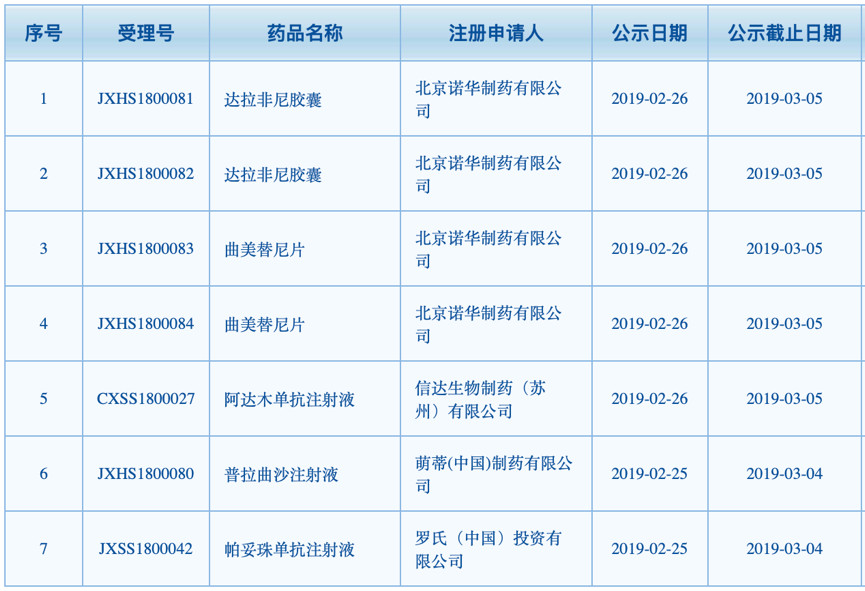
▍70億市場,,兩新藥提前上市?,!
據(jù)醫(yī)藥地理顯示,,達(dá)拉非尼和曲美替尼均為GSK研發(fā),現(xiàn)在歸諾華所有。起因在于2014-2015年GSK與諾華的業(yè)務(wù)大互換:當(dāng)時,,諾華以145億美元收購GSK的腫瘤業(yè)務(wù),,而諾華也將把除流感疫苗之外的疫苗業(yè)務(wù),以71億美元加專利使用費(fèi)的價格轉(zhuǎn)讓給GSK,。
資料顯示,,達(dá)拉非尼,F(xiàn)DA于2013年批準(zhǔn)了其用于治療轉(zhuǎn)移性黑色素瘤和不能行手術(shù)治療的黑色素瘤病人,。是繼維羅非尼,、易普利單抗后批準(zhǔn)的第三個治療轉(zhuǎn)移性黑色素瘤藥物,而曲美替尼用于攜帶BRAF V600E/K突變的晚期黑色素瘤患者,,是FDA批準(zhǔn)的第一個激酶別構(gòu)抑制劑,。
根據(jù)藥物綜合數(shù)據(jù)庫(PDB)顯示,2014-2017年達(dá)拉非尼一直保持穩(wěn)步增長,,2017年全球銷售額近6億美元,,在經(jīng)過2015年55%的高速增長后,2016~2017年逐漸趨于穩(wěn)定,。

(圖片來源:醫(yī)藥地理)
根據(jù)藥物綜合數(shù)據(jù)庫(PDB)顯示,,2014-2017年曲美替尼則一直保持高速增長,2017年全球銷售額近5億美元,,增長率在2016年經(jīng)歷了一個較大波動后,,2017年又恢復(fù)了64%的高速增長。

(圖片來源:醫(yī)藥地理)
總的來說,,兩款新藥在全球有近11億美元(約人民幣73億)的市場份額,,并且還保持著不低的增長速率,在中國可能會有較大的市場前景,。
▍國產(chǎn)修美樂,,第三家要來了?,!
資料顯示,,信達(dá)提交阿達(dá)木單抗類似物上市申請,是修美樂的生物類似藥,,進(jìn)度排名國內(nèi)第三,,前兩家分別是百奧泰和海正藥業(yè)。
原研藥修美樂(阿達(dá)木單抗注射液)是全球首個獲批上市的全人源抗腫瘤壞死因子單克隆抗體,,在全球獲批的適應(yīng)癥多達(dá)14個,,有“全球藥王”之稱。
但顯然,,中國不太買賬“藥王”的稱號,,根據(jù)米內(nèi)網(wǎng)中國公立醫(yī)療機(jī)構(gòu)終端競爭格局?jǐn)?shù)據(jù)顯示,,阿達(dá)木單抗2017年銷售額為8125萬,遠(yuǎn)低于同靶點(diǎn)藥物益賽普(注射用重組人Ⅱ型腫瘤壞死因子受體抗體融合蛋白)的銷售額,。
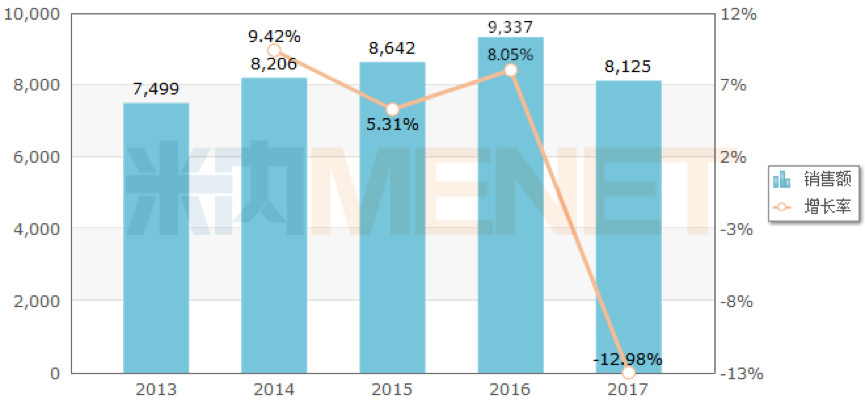
(圖片來源:米內(nèi)網(wǎng))
▍正大天晴,、恒瑞、豪森新藥受理號TOP3
中國的市場環(huán)境較為復(fù)雜,,藥品研發(fā)容易受到技術(shù),、審批、政策等多方面因素的影響,,存在較多的不確定因素,。為改革藥品審評審批制度,解決藥品審評積壓的狀況,。2016年2月26日,,原國家食藥監(jiān)局頒布了《關(guān)于解決藥品注冊申請積壓實(shí)行優(yōu)先審評審批的意見》。
因此,,2016年是優(yōu)先審評審批的關(guān)鍵年,。據(jù)藥智網(wǎng)數(shù)據(jù),,截止2019年2月23日,,納入優(yōu)先審評的藥品受理號達(dá)791個。其中仿制藥申報占比最多,,為39.70%,,其次為新藥,約有三分之一的占比,。
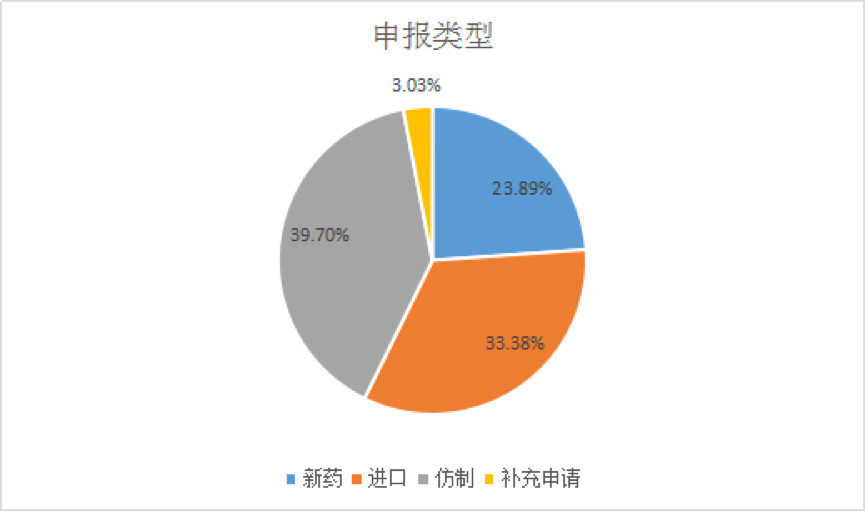
(圖片來源:藥智網(wǎng))
按照申報類型進(jìn)行分類,,可以分為新藥、仿制藥,、進(jìn)口藥三類,。
其中,新藥的理由有重大專項(xiàng),、具有明顯臨床價值的創(chuàng)新藥,、具有明顯治療優(yōu)勢的新藥,藥智網(wǎng)數(shù)據(jù)顯示,,列入優(yōu)先審評的新藥受理號總計(jì)達(dá)189個,。
在申報新藥的企業(yè)中,正大天晴的受理數(shù)最多,,為17個,,恒瑞醫(yī)藥和豪森藥業(yè)次之,分別為12個和8個,。
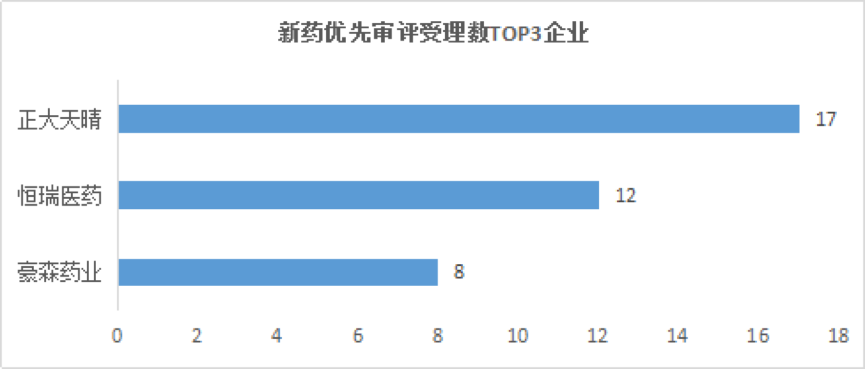
(圖片來源:藥智網(wǎng))
擁有首仿產(chǎn)品,、貢獻(xiàn)產(chǎn)品兒童用藥,、與現(xiàn)有治療手段相比具有明顯治療優(yōu)勢藥品等理由的仿制藥會列入優(yōu)先審評審批,目前的仿制藥受理號總計(jì)315個,,浙江華海,、東陽光藥業(yè)、齊魯制藥為申報企業(yè)TOP3,。
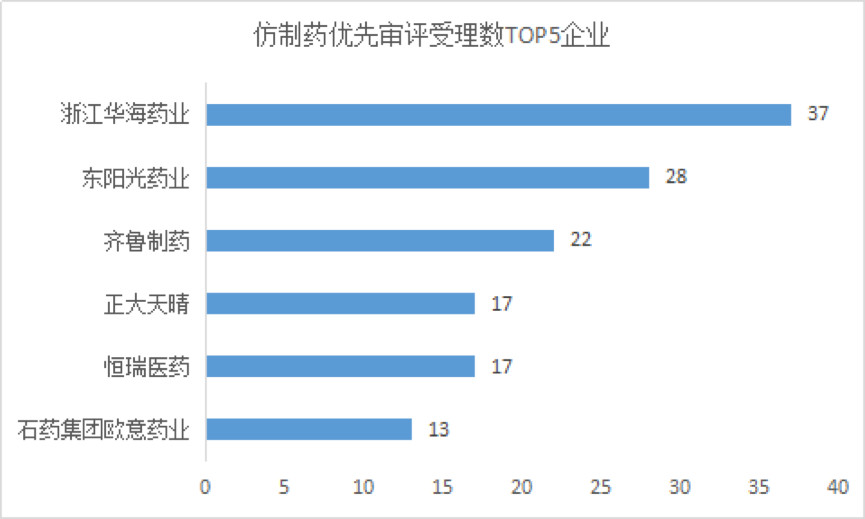
(圖片來源:藥智網(wǎng))
在進(jìn)口藥的申報理由中,,多是腫瘤藥、臨床急需藥品,、罕見病藥等,。進(jìn)口藥申請受理號達(dá)263個,申報企業(yè)TOP3分別為拜耳,、諾華,、勃林格殷格翰。
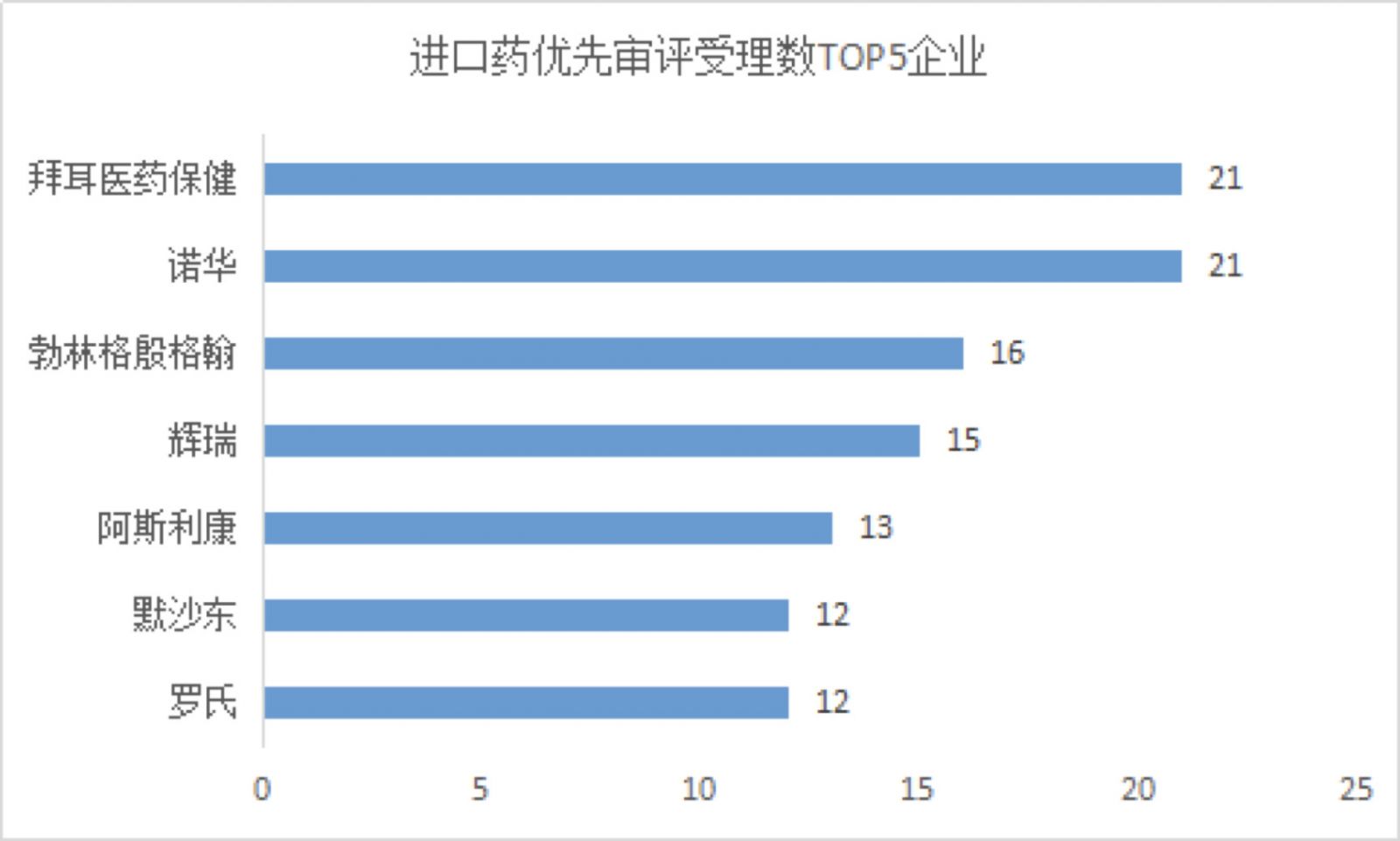
(圖片來源:藥智網(wǎng))







