2月17日,,國家局公布藥品批準(zhǔn)文號信息,,長春海悅他達(dá)拉非片首仿獲批上市。
▍重磅藥,,首仿上市
長春海悅藥業(yè)在 2017 年 7 月 10 日申報生產(chǎn),,2017 年 11 月 22 日被 CDE 納入優(yōu)先審評,2019 年 2月獲批上市,,該藥品按照新 4 類申報,,此次通過也意味著視同通過一致性評價。

(圖片來源:Insight數(shù)據(jù)庫)
他達(dá)拉非,,商品名:希愛力(Cialis),,是禮來開發(fā)的長效磷酸二酯酶 5(PDE5)抑制劑,用于治療男性勃起功能障礙(ED),。
2003 年在美國上市,, 2016 年全球銷售業(yè)績?yōu)?24.56 億美元,2017 年為 23.04 億美元,。
據(jù)米內(nèi)網(wǎng)數(shù)據(jù)顯示,,2017年在中國城市公立醫(yī)院、縣級公立醫(yī)院,、城市社區(qū)中心、鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機(jī)構(gòu))終端及中國城市零售藥店終端化學(xué)藥市場中,,他達(dá)拉非的合計銷售額超過7億元,。
▍ED三款主要治療藥物
ED一線治療方案主要是口服藥物治療,臨床上常用的藥物是5型磷酸二酯酶抑制劑(PDE5),,目前已經(jīng)上市的PDE5抑制劑有西地那非,、他達(dá)拉非、伐地那非等,。
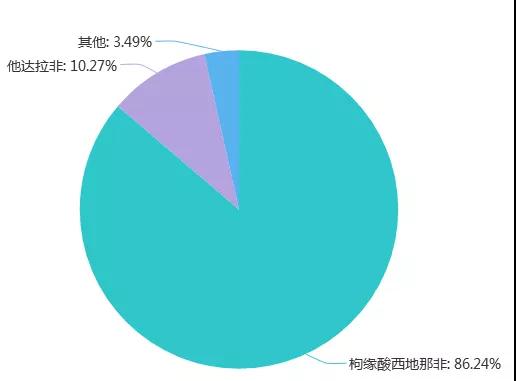
(圖片來源:新康界)
中康CMH數(shù)據(jù)顯示,,2017年我國枸緣酸西地那非、他達(dá)拉非片總銷售額為34.03億元(僅為線下醫(yī)院及藥店銷售總額,,不含網(wǎng)上藥店銷售額),。
中國市場除枸緣酸西地那非和他達(dá)拉非之外,加上甲磺酸酚妥拉明,、鹽酸阿撲嗎啡,、鹽酸達(dá)泊西汀、鹽酸伐地那非等抗ED用藥,,整個抗ED用藥市場約35.27億元,。
萬艾可(西地那非)
輝瑞的萬艾可(西地那非)是抗ED領(lǐng)域的開山鼻祖,1998年在美國獲批上市后銷售額一直穩(wěn)步上漲,,其中銷售高峰出現(xiàn)在2012年,,當(dāng)年的全球銷售額為20.51億美元,。隨著產(chǎn)品在各國的專利陸續(xù)到期,萬艾可受到了仿制藥的不斷沖擊,,銷量銳減,,2017年全球銷售額下滑至12.04億美元。
希愛力(他達(dá)拉非)
禮來的希愛力(他達(dá)拉非)在2002年獲批,,2003年在法國上市,。上市初期成績雖不如萬艾可,但從2007年起,,其增長速度開始變得迅猛,,2017年的全球銷售額達(dá)到了23.23億美元。希愛力的化合物專利在2015年1月到期,,但ED用途專利2020年4月才到期,,預(yù)計未來幾年的全球銷售額仍然有上漲的潛力。
艾力達(dá)(伐地那非)
拜耳的艾力達(dá)(伐地那非)在2003年推出市場,,但相比輝瑞和禮來,,拜耳對市場布局魄力相對不足,上市后的成績單并不亮眼,,2015年全球銷售額僅為2.26億歐元(約為2.64億美元),。相比萬艾可和希愛力,艾力達(dá)的起效時間最快,,約15分鐘左右,,有效時間與萬艾可相似,約4~5小時,。
▍27家仿制藥在研
ED的市場一直十分被看好,,輝瑞,即使專利過期,,2017年全球銷售額還是高達(dá)12.04億美元,。而他達(dá)拉非的市場潛力則更為可觀。
據(jù)藥渡分析,,雖然他達(dá)拉非上市晚于西地那非,,但是2013年之后,他達(dá)拉非的銷售額就反超“偉哥”,,2018年他達(dá)拉非的全球市場銷售額超過西地那非近10億美元,。
他達(dá)拉非首先于2002年獲歐洲EMA批準(zhǔn),次年獲美國FDA獲批,,進(jìn)入中國已是2004年,。
一開始,他達(dá)拉非并沒有表現(xiàn)出特別的競爭力,直到2007年6月和2008年1月,,他達(dá)拉非先后在歐洲和美國成功獲批“once daily use”(每日一次)劑型,,至此在全球范圍內(nèi)開啟了ED治療的新模式
他達(dá)拉非每日一次服用,使患者擺脫了“計劃”和“時間”的束縛,。隨后2013年他達(dá)拉非“once daily use”在國內(nèi)也成功獲批上市,。
有評論指出,盡管他達(dá)拉非目前在全球的銷售額遠(yuǎn)超西地那非,,但在中國市場上,,西地那非的份額仍相對領(lǐng)先,這可能和西地那非的仿制藥低價優(yōu)勢有關(guān),,隨著他達(dá)拉非的仿制藥陸續(xù)獲批,,其市場份額也有望進(jìn)一步增長。
據(jù)insight數(shù)據(jù)庫信息,,目前,,國內(nèi)他達(dá)拉非片劑僅 2 家企業(yè)批準(zhǔn)上市,但在研廠家多達(dá) 27 家,,可見競爭不小,。







